ТИРЕОИДНЫЕ ГОРМОНЫ
Тиреоидные гормоны оказывают многочисленные и разнообразные эффекты на дифференцировку, развитие и метаболический гомеостаз, контролируя синтез и активность регуляторных белков, в том числе ключевых ферментов метаболизма, гормонов и рецепторов. Известное действие тиреоидных гормонов на потребление кислорода определяется отчасти стимуляцией натриевого насоса за счет индукции мембранного фермента: натрий-, калийзависимой АТФазы [110а]. Этот и другие метаболические эффекты тиреоидных гормонов зависят от гормональной индукции синтеза РНК, осуществляемой путем регуляции экспрессии генов на ядерном уровне. Хотя постулировались прямые влияния тиреоидных гормонов и на клеточную мембрану и на митохондрии, но многие из эффектов этих гормонов на процессы метаболизма опосредуются, по-видимому, активацией ядерных реакций связывания с увеличением образования специфических РНК.
Основным йодтиронином, секретируемым щитовидной железой, является тироксин (Т4), которому сопутствует небольшое количество активного трийодтиронина (Т3). В тканях-мишенях Т4 дейодируется в Т3, который представляет собой главную внутриклеточную форму гормона. Это превращение происходит на плазматической мембране и в эндоплазматическом ретикулуме, и в разных тканях варьирует по степени, будучи интенсивным в передней доле гипофиза и менее выраженным в печени и почках. Большая зависимость гипофиза от превращения циркулирующего в крови Т4 в Т3 могла бы определяться потребностью в быстром увеличении гипофизарной продукции ТТГ при небольших изменениях в секреции Т4 щитовидной железой.
Большая часть циркулирующих в крови тиреоидных гормонов связана с белками плазмы: тироксинсвязывающим глобулином (ТСГ), тироксинсвязывающим преальбумином (ТСПА) и альбумином. Все они связывают Т4 более прочно, чем Т3, причем ТСГ переносит около 70% связанного Т4 плазмы; из остального количества около 10% связано с ТСПА, а 20% с альбумином [111]. Как и в отношении стероидных гормонов, именно свободные тиреоидные гормоны ответственны за контроль активности клеток-мишеней, и функция связывающих белков, помимо того, что они являются резервуаром циркулирующего гормона, неясна. Интересной особенностью ТСПА является то, что он в некоторых отношениях напоминает клеточный рецептор тиреоидного гормона, в том числе присутствием предположительного ДНК-связывающего участка, богатого заряженными аминокислотами и триптофановыми остатками.
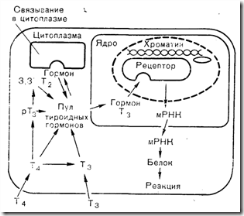
Рис. 4—29. Эффекты и взаимопревращение Т4 и Т3 В клетках, реагирующих на поступление тиреоидных гормонов. Процесс активации ядра зависит от связывания Т3 с ядерными рецепторами, а не от отдельно существующих цитоплазматических рецепторов, как это имеет место в клетках-мишенях стероидных гормонов (Eberhardt и соавт. [111] в модификации).
Клеточные рецепторы тиреоидных гормонов
Хотя показано присутствие связывающих Т3 белков в цитоплазме, но они обладают относительно низким сродством по сравнению с ядерными участками, которые считаются в настоящее время истинными рецепторами, ответственными за эффекты тиреоидных гормонов [112]. Так, в отличие от стероидных гормонов, тиреоидные гормоны, по-видимому, не нуждаются во взаимодействии с цитозольными рецепторами для последующей транслокации в ядро (рис. 4—29). Ядерные участки связывания Т3 обладают высоким сродством и низкой емкостью и ассоциированы с ядерными негистоновыми белками; их молекулярная масса после солюбилизации составляет примерно 50000 [111]. Они присутствуют во всех гормончувствительных тканях (печень, почки, сердце и гипофиз) и отсутствуют в тканях, не реагирующих на тиреоидные гормоны (семенники, селезенка), и, возможно, в тканях больных с семейной резистентностью к тиреоидным гормонам. Ядерное связывание многочисленных аналогов Т3 тесно коррелирует с их биологической активностью, а вслед за насыщением рецепторов происходит увеличение активности полимеразы и образования РНК.
Ядерные эффекты тиреоидных гормонов
Стимуляция ядерных процессов тиреоидными гормонами была впервые установлена Tata [114]; она включает повышенное образование высокомолекулярных яРНК и мРНК, как и в случае стероидных гормонов. У животных с гипотиреозом скорость образования как предшественника РНК, так и мРНК снижена на 40%, но она быстро восстанавливается до нормы после введения Т3. Помимо своих генерализованных эффектов на геном, Т3 оказывает также избирательное действие на мРНК, кодирующий a2-макроглобулпн в печени и СТГ в клетках гипофиза. Вероятно, стимулирующее действие Т3 на активность других белков, таких, как митохондриальный фермент a-глицерофосфатдегидрогеназа (a-ГФД) и цитоплазматический маликфермент, также опосредуется повышением синтеза специфических мРНК [ИЗ].
Общие особенности действия тиреоидных гормонов в разных тканях проявляются в разной степени как из-за видовой и тканевой специфичности эффектов, так и из-за индивидуальных различий в зависимости между насыщенностью рецепторов и биологическими реакциями. Так, влияния Т3 на a-ГФД и маликфермент заметно варьируют в разных тканях и у разных видов животных, причем каждая ткань, по-видимому, реагирует на Т3 индивидуально [113]. Другой особенностью действия Т3 является его участие в мультигормональной регуляции синтеза мРНК. Это наглядно проявляется на примере продукции a2-макроглобулиновой мРНК, на которую влияют кортизол, андрогены и СТГ, равно как и Т3. Кортизол и Т3 оказывают также синергичное действие на синтез мРНК гормона роста в клетках гипофиза. Наконец, метаболические факторы также модифицируют влияния Т3 на экспрессию отдельных генов, что проявляется особенно отчетливо при голодании и после введения углеводов. Так, индукция маликфермента под влиянием Т3 зависит от приема углеводов и не происходит при голодании. Однако голодание не препятствует реакции a-ГФД на Т3, что опять-таки свидетельствует о значении местных клеточных факторов в проявлении эффектов тиреоидных гормонов [113]. Очевидно, что большинство модуляций эффектов тиреоидных гормонов в отдельных тканях и в разных физиологических условиях могло бы происходить на пострецепторном уровне, реализуясь путем изменения скорости синтеза и процессинга мРНК в ядре и их последующей трансляции в специфические белки в цитоплазме


