ОБЩАЯ ТОКСИКОЛОГИЯ
Основные понятия токсикологии
Введение
Ответить на вопрос о первой встрече с ядами человека весьма затруднительно: она состоялась в те далекие времена, когда наши предки впервые сталкивались с ядовитыми насекомыми, животными и растениями. Действие ядов было покрыто тайной и объяснялось связью с черной магией и злыми духами. Пользоваться ядами для охоты на животных, а затем с преступной и лечебной целью люди научились задолго до того, как поняли более менее механизм действия ядовитых веществ.
В качестве ядов использовались высокотоксичные вещества растительного происхождения: алкалоиды и глюкозиды (стрихнин, кураре, аканид, страфантин, белена, дурман и т.д.). Наиболее широко отравления использовались в политической борьбе и частной жизни во времена средневековья. Чаще всего применяли мышьяк, который составил целую эпоху применения ядов в криминальных целях, став причиной смерти многих тысяч жертв необузданных страстей и коварных замыслов. Массу примеров применения ядов с преступной целью можно найти в литературе («Моцарт и Сальери» А.С. Пушкина, «Граф Монте-Кристо» Дюма и др.)
С развитием химических наук были открыты механизмы действия химических веществ, и яды потеряли свое мистическое значение. Но появилось много синтетических веществ, большинство из которых оказались высокотоксичными. Они широко используются в промышленности, сельском хозяйстве, медицине, быту.
И это создает новую экологическую опасность для здоровья людей.
Изучение токсичности применяемых на производстве и в быту химических веществ, механизм их воздействия на организм человека, разработка противоядий, мер профилактики с целью предупреждения отравлений и входит в задачу науки токсикологии. Специалисты в области охраны окружающей среды должны быть информированы о токсичности химических веществ, иметь представление о взаимосвязи токсичности и структуры, о путях биотрансформации ядов в организме, уметь рассчитать ПДК вредных веществ.
С этой целью и предлагается данное пособие будущим инженерам-экологам. Пособие содержит как отдельные теоретические вопросы, так и лабораторные работы по обнаружению токсичных катионов и анионов, а также токсичных органических веществ различными методами. Уметь предсказать возможные последствия применения синтетических материалов на здоровье людей и состояние окружающей среды.
Предмет и задачи токсикологии
Токсикология (от греческого toxicon – яд и logos – учение) – это наука, изучающая законы взаимодействия живого организма и яда. В роли последнего может оказаться практически любое химическое соединение, попавшее в организм в количестве, способном вызвать нарушения жизненно важных функций и создать опасность для жизни.
Знаменитый врач древности Парацельс (1493-1541 гг. жизни) считал, что «все есть яд, и ничто не лишено ядовитости». С другой стороны, давно известно, что многие химические вещества, принятые внутрь в оптимальной дозе, приводят к восстановлению нарушенных какой-либо болезнью функций организма и тем самым проявляют лечебные свойства. В этом отношении токсикология тесно связана с фармакологией – наукой о действиях лекарств на организм. Кроме того, многие вещества сами являются составной частью живого организма, – это белки, жиры, углеводы и пр., и для проявления их токсических свойств нужны особые условия. Чаще токсическое действие оказывают чуждые живому организму вещества, которые получили название «ксенобиотики» (от греческого xenos – чуждый).
Некоторые вещества, находясь в определенном количестве в среде обитания или внутренней среде организма человека и животных, составляют обязательное условие их существования, например микроэлементы (серебро, йод, кобальт и др.).
Таким образом, одно и тоже химическое вещество может быть ядом, лекарством и необходимым для жизни средством, в зависимости от ряда условий, при которых оно встречается и взаимодействует с организмом.
Основная задача токсикологии – обнаружение и характеристика токсических свойств химических веществ, которые способны вызвать в организме патологические изменения, а также изучение условий, при которых эти свойства возникают, ярко проявляются и исчезают.
Второй важной задачей токсикологии является определение зоны токсического действия изучаемого химического вещества.
Третья задача токсикологии предусматривает изучение химических и патоморфологических признаков отравления при различных путях поступления ядов в организм.
Показатели токсичности зависят не только от свойств яда, но и от вида, пола, возраста, индивидуальной чувствительности к нему организма. Отсюда вытекает еще одна важная задача токсикологии – разработка основ экстраполяции на человека данных, изученных в эксперименте на животных.
Токсикология является фундаментальной наукой, которая решает широкий круг задач, привлекая знание многих смежных естественных наук: неорганической, органической химии, биохимии, физиологии, иммунологии и генетики. Основным методологическим приемом в токсикологии является эксперимент на животных. Он должен быть технически хорошо оснащен, чтобы выявить наиболее тонкий механизм действия ядов на организм в целом, на орган отдельно, на клеточном и молекулярном уровнях.
Основные разделы токсикологии
В настоящее время в токсикологии определяются три основных направления; теоретическое (экспериментальное), профилактическое (гигиеническое) и клиническое.
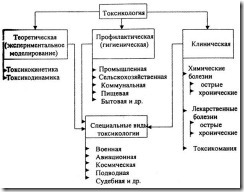 |
Схема 1. Основные разделы токсикологии.
Теоретическая токсикология решает проблемы выявления основных законов взаимодействия организмов и ядов. Она включает два основных раздела:
1) токсикодинамику, которая рассматривает действие яда на организм;
2) токсикокинетику, которая изучает ответную реакцию организма на яд. Это происходит во времени, с разной скоростью.
Профилактическая токсикология изучает проблемы определения степени опасности и разработку мер и способов предотвращения и защиты от токсического воздействия химических веществ в окружающей человека среде. Поэтому она имеет экологический характер и включает следующие основные разделы: промышленный, сельскохозяйственный, коммунальный, пищевой, бытовой и др.
Клиническая токсикология исследует заболевания химической этиологии, т.е. болезни человека, возникающие вследствие токсического влияния химических соединений окружающей его среды.
Кроме того, выделяются специальные виды токсикологии, которые изучают отравление людей в любых условиях или обстоятельствах при воздействии определенного типа токсических веществ. Это военная, авиационная, космическая, судебная и прочие виды токсикологии, которые обычно включают в себя элементы всех основных направлений – теоретического, гигиенического и клинического.
Для будущих инженеров наибольший интерес представляет промышленная токсикология, задачами которой являются:
- гигиеническое нормирование содержания вредных веществ в объектах производственной среды и биосредах;
- гигиеническая экспертиза токсичных веществ;
- гигиеническая стандартизация сырья и продуктов.
Гигиеническое нормирование ограничивает содержание вредных веществ путем установления предельно допустимых концентраций в воздухе рабочей зоны и на коже. Гигиеническая экспертиза представляет собой наиболее массовый вид токсикологической оценки вредных веществ, предусматривающий определение смертельных доз и концентраций при различных путях введения, адекватным путям поступления ядов в производственных условиях. Гигиеническая стандартизация сырья и продуктов предполагает ограниченное содержание токсичных примесей в промышленном сырье и готовых продуктах с учетом их вредности и опасности.
Основные понятия токсикологии
В токсикологии наиболее часто приходится оперировать определенными понятиями, например, терминами «яд» и «токсин». К ядам токсикологи относят химические соединения, способные в минимальных количествах вызывать тяжелые нарушения жизнедеятельности (отравления) или гибель животного организма. Токсинами традиционно называют белковые вещества, образуемые преимущественно микроорганизмами, растениями и животными, которые обладают ядовитым действием. В настоящее время термин «токсин» чаще всего относят к индивидуальному химическому веществу, выделенного из того или иного яда или тканей ядовитого организма. Термин «яд» обычно применяют к секретам ядовитых желез животных (змей, насекомых и пр.). В свою очередь слово «токсин» широко используется при образовании новых терминов, подчеркивающих источник происхождения данного токсина (зоотоксины, фитотоксины), либо особенности его физиологического или фармакологического эффекта (нейротоксины, кардиотоксины).
По своей химической структуре токсины природного происхождения весьма разнообразны. В их числе можно встретить алифатические и гетероциклические, алкалоиды, стероиды, ферментативные белки. Некоторые из этих соединений можно условно назвать «истинными токсинами» в том смысле, что они не встречаются в организме реципиента и является для него ксенобиотики (чужеродными веществами). Другая группа компонентов природных ядов образованы химическими веществами, которые встречаются и в организме реципиента. К ним относятся ацетилхолин, гистамин, катехоламины (адреналин, норадреналин), производные индола, различные ферменты и их ингибиторы. Токсический эффект этих соединений определяется избыточностью дозировки, значительно превышающей физиологические пределы их действующих концентраций в организме.
Биологическое значение зоотоксинов для их продуцентов связано с использованием ядов как оружия защиты или нападения. Защитное действие реализуется с помощью различных механизмов: болевого, репеллентного (отпугивающего) и некоторых других. При нападении на жертву на первый план выступает паралитическое (обездвиживающее) действие.
Токсикант – вещество антропогенного происхождения, способное при попадании в организм вызывать заболевание или гибель.
Токсичность – способность вещества вызывать в организме нарушение физиологических функций или его гибель.
Толерантность – способность организма переносить воздействие яда без развития токсического эффекта.
Вредное вещество – вещество, которое при контакте с организмом человека в случае нарушения требований безопасности может вызвать производственные травмы, профессиональные заболевания или отклонения в состоянии здоровья, обнаруживаемые современными методами, как в процессе работы, так и в отдаленные сроки жизни настоящего и последующих поколений.
Опасное вещество – потенциально вредное вещество, т.е. вещество, которое может проявить свои вредные свойства в определенных условиях.
Принципы классификации ядов
Количество химических соединений, используемых в настоящее время, настолько велико, а характер их биологического действия настолько разнообразен, что приходится применять несколько видов классификации. Они делятся на две группы: общие, основанные на каком-либо общем принципе оценки, подходящем для всех без исключения химических веществ, и специальные, отражающие связь между отдельными физико-химическими или другими признаками веществ и проявлениями их токсичности.
Принципы классификации ядов табл. 1
|
Общие |
Специальные |
|
– По химическим свойствам (химическая) – По цели применения (практическая) – По степени токсичности (гигиеническая) – По виду токсического действия (токсикологическая) – По избирательной токсичности |
– По типу развивающейся гипоксии (патофизиологическая) – По механизму взаимодействия с ферментными системами (патохимическая) –По характеру биологических последствий отравлений (биологическая) – По степени канцерогенной активности и др. |
Наиболее широко используется химическая классификация, предусматривающая деление всех химических веществ на органические, неорганические и элементоорганические. Исходя из принятой химической номенклатуры, определяют класс и группу этих веществ.
Большое значение для профилактики отравлений имеет классификация токсичных веществ по цели применения. По этому признаку различают:
- промышленные яды, используемые в промышленной среде. Среди них органические растворители, топливо, красители, хладореагенты, химреагенты, пластификаторы и др.
- ядохимикаты, используемые в сельском хозяйстве.
- лекарственные средства, имеющие свою классификацию.
- бытовые химикалии, используемые в быту современного человека в виде пищевых добавок, средств санитарии, личной гигиены и косметики, средств по уходу за одеждой, мебелью, автомобилем и пр.
- биологические и растительные яды, которые содержатся в различных растениях и грибах, животных и насекомых и вызывают отравление при попадании в организм.
- боевые отравляющие вещества, которые применяются в качестве токсического оружия как средства ведения химической войны (БОВ).
Для клинической токсикологии наибольшее значение имеет разделение химических веществ по характеру взаимодействия на организм. Это позволяет поставить первичный клинический диагноз, разработать принципы профилактики и лечения токсического поражения и определить механизм его развития.
Токсикологическая классификация ядов
1. Нервно-паралитическое действие (бронхоспазм, удушье, судороги и параличи): фосфорорганические инсектициды (хлорофос, карбофос), никотин, анабазин, БОВ (зарин и пр.).
2. Кожно-резорбтивное действие (местные воспалительные и некротические изменения в сочетании с общетоксическими резорбтивными явлениями): дихлорэтан, гексахлоран, БОВ (иприт, люизит), уксусная эссенция, мышьяк и его соединения, ртуть (сулема).
3. Общетоксическое действие (гипоксические судороги, кома, отек мозга, параличи): синильная кислота и ее производные, угарный газ, алкоголь и его суррогаты, БОВ (хлорциан).
4. Удушающее действие (токсический отек легких): оксиды азота, БОВ (фосген, дифосген).
5. Слезоточивое и раздражающее действие (раздражение наружных слизистых оболочек): хлорпикрин, БОВ (адамсит), пары крепких кислот и щелочей.
6. Психическое действие (нарушение психической активности, сознания): наркотики (кокаин, опий), атропин, БОВ (ЛСД, диэтиламид).
Однако токсикологическая классификация ядов имеет общий характер и обычно детализируется за счет дополнительной информации об их избирательной токсичности.
Классификация ядов по избирательной токсичности
1. Сердечные яды (кардиологическое действие – нарушение ритма и проводимости сердца, токсическая дистрофия миокарда): сердечные гликозиды (дигиталис, дигоксин); трициклические антидепрессанты (имипрамин, амитриптилин); растительные яды (аконит, чемерица, заманиха); животные яды (тетрадоксин); соли бария.
2. Нервные яды (нейротоксическое действие – нарушение психической активности, токсическая кома, токсические гиперкинезы и параличи): психофармакологические средства (наркотики, транквилизаторы, снотворные); фосфорорганические соединения; угарный газ; производные изониазида (тубазид, фтивазид); алкоголь и его суррогаты.
3. Печеночные яды (гепатотоксическое действие – токсическая гепатопатия): хлорированные углеводороды (дихлорэтан); ядовитые грибы; фенолы и альдегиды.
4. Почечные яды (нефротоксическое действие – токсическая нефропатия): соединения тяжелых металлов; этиленгликоль, щавелевая кислота.
5. Кровяные яды (гематотоксическое действие – гемолиз, метгемоглобинемия): анилин и его производные; нитриты; мышьяковистый водород.
6. Желудочно-кишечные яды (гастроэнтеротоксическое действие – токсический гастроэнтерит): крепкие кислоты и щелочи; соединения тяжелых металлов и мышьяка.
Следует иметь в виду, что избирательное токсическое действие яда не исчерпывает всего многообразия клинических проявлений интоксикации, а лишь указывает на непосредственную опасность, которая грозит определенному органу или системе организма как основному месту токсического поражения.
Специальные принципы классификации вредных веществ представляют в основном интерес для медицины.
Классификация промышленных ядов
К промышленным ядам относится большая группа химических веществ и соединений, которые в виде сырья, промежуточных или готовых продуктов встречаются на производстве.
Наиболее частое применение находят классификации промышленных ядов по классам химических соединений, по характеру воздействия на организм, по степени воздействия на организм.
По характеру воздействия на организм вещества подразделяются:
- на общетоксические – вызывающие отравления всего организма или поражающие отдельные системы, а также вызывающие патологические изменения печени и почек (угарный газ, свинец, ртуть, бензол);
- раздражающие – вызывающие раздражения слизистых оболочек дыхательных путей, глаз, легких, кожных покровов (хлор, аммиак, оксиды серы и азота, озон);
- сенсибилизирующие – действующие как аллергены (формальдегид, растворители, нитролаки);
- мутагенные – приводящие к нарушению генетического кода, изменению наследственной информации (свинец, марганец, радиоактивные изотопы);
- канцерогенные – вызывающие злокачественные новообразования (ароматические углеводороды, хром, никель, асбест);
- влияющие на репродуктивную функцию (ртуть, свинец, стирол);
Три последних вида воздействия вредных веществ – мутагенное канцерогенное, влияние на репродуктивную функцию, а также ускорение старения, относят к отдаленным последствиям влияния химических соединений на организм. Это специфическое действие, которое проявляется спустя годы, и даже десятилетия.
Эта классификация не учитывает агрегатного состояния веществ, тогда как для большой группы аэрозолей, не обладающих выраженной токсичностью, следует выделить фиброгенный эффект действия на организм. К ним относятся аэрозоли дезинтеграции угля, аэрозоли кокса, алмазов, пыли животного и растительного происхождения, силикатосодержащие пыли, алюмосиликаты, аэрозоли дезинтеграции и конденсации металлов.
Попадая в органы дыхания, вещества этой группы вызывают атрофию или гипертрофию слизистой верхних дыхательных путей, а, задерживаясь в легких, приводят к развитию соединительной ткани в воздухообменной зоне и рубцеванию легких. Наличие фиброгенного эффекта не исключает общетоксического действия аэрозолей.
По пути проникновения в организм различают вещества, попадающие в органы дыхания, желудочно-кишечный тракт, неповрежденную кожу.
Классификация пестицидов
По производственному назначению пестициды (вещества, применяемые для борьбы с вредными организмами) подразделяются на следующие группы:
- акарициды – средства для борьбы с клещами;
- арборициды – средства для уничтожения нежелательных кустарников и деревьев;
- альгициды – средства для уничтожения водорослей в водоемах;
- аттрактанты – вещества, привлекающие насекомых;
- афициды – средства для борьбы с тлями;
- гербициды – средства для борьбы с вредными растениями;
- дефолианты – средства для удаления листьев с технических культур при машинной обработке урожая;
- десиканты – средства для подсушивания растений;
- зооциды – средства для борьбы с грызунами;
- инсектициды – средства для борьбы с вредными насекомыми;
- ихтиоциды – средства для борьбы с сорными видами рыб;
- ларвициды – средства для уничтожения личинок и гусениц;
- моллюскоциды – средства для борьбы с моллюсками и слизнями;
- нематоциды – средства для борьбы с круглыми червями;
- овициды – средства для уничтожения яиц насекомых;
- реторданты – регуляторы роста растений;
- репелленты – средства для отпугивания летающих насекомых;
- фунгициды – средства для борьбы с грибами;
- хемостерилянты – средства для стерилизации самцов и самок вредных насекомых.
По химическому составу пестициды подразделяют на фосфорорганические, хлорорганические, карбаматные, ртутноорганические, производные хлорфеноксиуксусной кислоты, производные мочевины, производные триазина, гетероциклические соединения, нитро- и хлорпроизводные фенола, медьсодержащие соединения, циан- и родансодержащие соединения, фторсодержащие соединения.
Гигиеническая классификация пестицидов включает следующие основные критерии вредности: токсичность по величине среднесмертной дозы при однократном введении в желудок, кожно-резорбтивную токсичность, кумулятивные свойства, опасность веществ по степени летучести, стойкость во внешней среде, бластомогенность, тератогенность, эмбриотоксичность и аллергенные свойства пестицидов.
По стойкости во внешней среде пестициды делятся на четыре группы в зависимости от периода полураспада:
1) очень стойкие – 1-2 года;
2) стойкие – от 6 мес. до 1 года;
3) умеренно стойкие – 1-6 мес.;
4) малостойкие – до 1 мес.
По степени бластомогенности пестициды разделяются также на четыре группы:
1) явно канцерогенные (известно возникновение рака у людей);
2) канцерогенные (канцерогенность доказана на животных);
3) слабоканцерогенные (слабые канцерогены на животных);
4) подозрительные на бластомогенность.
По степени тератогенности пестициды делят на две группы:
1) явные тератогены (известные уродства у людей и животных);
2) подозрительные на тератогенность (наличие экспериментальных данных на животных).
По степени эмбриотоксичности пестициды подразделяют на вещества с избирательной токсичностью в нетоксичных дозах для материнского плода и вещества с умеренной эмбриотоксичностью, которая проявляется наряду с другими токсическими эффектами.
По выраженности аллергических свойств среди пестицидов различают сильные аллергены, вызывающие аллергическое состояние у отдельных индивидуумов.
Классификация отравлений
Отравления – группа заболеваний, обусловленных воздействием на организм ядов различного происхождения.
По причине возникновения отравления делятся на случайные и преднамеренные.
Случайные отравления развиваются независимо от воли пострадавшего вследствие самолечения и передозировки лекарственных средств (например, обезболивающих при болевом синдроме или снотворных при бессоннице).
Преднамеренные отравления связаны с осознанным применением вещества с целью самоубийства (суицидальные отравления) или криминальные убийства. В последнем случае яд может быть применен для развития у потерпевшего беспомощного состояния (в целях ограбления, изнасилования).
В зависимости от условий возникновения и особенностей течения различают острые и хронические отравления. Острые развиваются при одномоментном поступлении в организм токсической дозы и характеризуются острым началом и выраженными специфическими симптомами. Хронические отравления обусловлены длительным (часто прерывистым) поступлением яда в малых дозах. Заболевание начинается с появления малоспецифических симптомов.
Выделяют более редкие по своей распространенности подострые отравления, когда при однократном введении яда в организм развитие отравления очень замедлено и вызывает продолжительное расстройство здоровья.
Острые отравления. При неправильной с гигиенической точки зрения организации труда и отсутствии специальных мер профилактики промышленные яды могут вызывать профессиональные отравления. Острым профессиональным отравлением называется заболевание, возникающее после однократного кратковременного воздействия вредного вещества на работающего (не более чем в течение одной смены).
Острые отравления чаще бывают групповыми и происходят в результате поломок оборудования и аварий, грубых нарушений требований безопасности труда и промсанитарии, когда содержание вредного вещества значительно – в десятки и сотни раз превышает предельно допустимую концентрацию, принятую для производственных помещений. Такое отравление в крайних случаях может либо окончиться быстрым выздоровлением, либо оказаться смертельным.
Например, при чистке цистерн высокие концентрации паров бензина являются причиной чрезвычайно быстро наступающего отравления, которое может закончиться гибелью от паралича дыхательного центра, если пострадавшего сразу же не вынести на свежий воздух. Столь же быстрая гибель угрожает при вдыхании больших концентраций сероводорода, вызывающего тканевую аноксию. Однако в отличие от молниеносно наступающих исходов острого отравления парами бензина или сероводорода, острое и даже смертельное отравление бромистым метилом выявляется после скрытого периода длительностью не менее 6-8 часов. Позднее развиваются признаки отравления в виде подергиваний, эпилептиформных судорог, затем следует потеря сознания и смерть. Особенно коварными являются отравления окислами азота из-за длительного (дни и недели) латентного периода, после которого может развиться тяжелый, зачастую смертельный, отек легких. Стадия отравления, характеризующая отсутствием проявления соответствующих симптомов называется скрытым периодом отравления.
Во многих случаях следствием перенесенного острого отравления являются стойкие нарушения здоровья. Так, в течение месяцев и даже лет после острого отравления бромистым метилом может сохраниться неверная походка, повышенная утомляемость, забывчивость, ослабление зрения, парезы периферических нервов; после отравления сероуглеродом – расстройства чувствительности, нарушение рефлексов, дефекты зрения и расстройство психической деятельности.
Раздражающие пары и газы редко вызывают тяжелые острые отравления в связи с тем, что болезненное раздражение слизистых оболочек глаз и верхних дыхательных путей заставляет рабочих быстро покидать помещение. Кроме того, экссудативная фаза воспалительной реакции, вызванная раздражающими веществами, резко уменьшает возможность дальнейшего проникновения яда в организм. Однако массивные концентрации раздражающих газов могут привести к рефлекторной остановке дыхания со смертельным исходом. В случае выздоровления, как правило, у таких пострадавших развивается токсический пневмосклероз.
Хроническое отравление. Хроническим отравлением называется заболевание, развивающееся после систематического длительного воздействия малых концентраций или доз вредного вещества. Имеются в виду дозы, которые при однократном поступлении в организм не вызывают симптомов отравления. Отравление развивается вследствие накопления вредного вещества в организме (материальная кумуляция) или вызываемых им нарушений в организме (функциональная кумуляция). Хроническое отравление органов дыхания может быть следствием перенесенной однократной или нескольких острых интоксикаций.
К ядам, вызывающим хронические отравления в результате только функциональной кумуляции, относятся хлорированные углеводороды, бензол, бензины.
В производственных условиях одни яды могут вызвать как острые, так и хронические отравления (бензин, оксид углерода, бензол), другие же – только или преимущественно острые (синильная кислота) или хронические (свинец, марганец) отравления.
Для многих промышленных ядов характерны только хронические отравления. Причиной этого может быть тот факт, что концентрации этих ядов, вызывающие острое отравление, в производственных условиях практически недостижимы (таковы свинец, марганец, тринитротолуол, пары ртути). В других случаях хроническое отравление практически не может быть вызвано ядом из-за быстрого его расщепления в организме или выведения. Так, двухвалентное железо – парализующий яд, но оно чрезвычайно быстро окисляется в организме в трехвалентное комплексное соединение, и производственные отравления железом не встречаются.
Существуют яды, вызывающие только острые отравления, например синильная кислота. Хронические отравления этим ядом рассматриваются как результат ряда острых и тяжелых отравлений. Долгое время аналогичным образом рассматривали и хронические отравления окисью углерода. Однако в настоящее время возможность отравления ею твердо доказана. Следовательно, любой промышленный яд может вызвать хроническое профессиональное заболевание в результате либо длительного воздействия малых пороговых концентраций, либо в случае повторения легких острых отравлений.
При хроническом и остром отравлении одним и тем же вредным веществом могут быть повреждены разные органы и системы организма. Например, при остром отравлении бензолом в основном страдает нервная система и наблюдается наркотическое действие, при хроническом же поражается система кроветворения.
Промежуточное место между острыми и хроническими занимают подострые отравления, которые по симптоматике сходны с острыми отравлениями, но возникают после более длительного воздействия яда в меньших концентрациях.
Развитие отравления и его исход в определенной мере зависят от физического состояния организма. Так, мышечное напряжение, вызывая сдвиги в обмене веществ и увеличивая потребность в кислороде, может неблагоприятно отразиться на течении интоксикации, особенно ядами, вызывающими гипоксию. Если токсическому действию предшествовало переутомление и перенапряжение нервной системы, это может повысить чувствительность к вредным веществам, обладающим наркотическим влиянием. Ослабление сопротивляемости ко многим ядам отмечается у людей, страдающих заболеваниями печени и почек. Не вызывает также сомнений повышенная восприимчивость к воздействию специфических ингредиентов при поражении кроветворного аппарата, органов дыхания, расстройства обмена веществ и целом ряде других патологических состояний.
Производственные яды, помимо острого или хронического отравления, могут оказать так называемое общее, неспецифическое действие – понижение общей неспецифической сопротивляемости вредным воздействиям, в частности инфекциям.
При повторном воздействии возможен эффект сенсибилизации – состояние организма, при котором повторное действие вещества вызывает больший эффект, чем предыдущее. Эффект сенсибилизации связан с образованием в крови и других внутренних средах измененных и ставших чужеродными для организма белковых молекул, индуцирующих образование антител. Повторное, даже более слабое токсическое воздействие с последующей реакцией яда с антителами вызывает неадекватный ответ организма в виде явлений сенсибилизации. Более того, в случае предварительной сенсибилизации возможно развитие аллергических реакций, выраженность которых зависит не столько от дозы воздействующего вещества, сколько от состояния организма. Аллергизация значительно осложняет течение острых и хронических интоксикаций, нередко приводя к ограничению трудоспособности. К веществам, вызывающим сенсибилизацию, относятся бериллий и его соединения, карбонилы никеля, железа, кобальта и соединения ванадия.
Параметры и основные закономерности токсикометрии
Экспериментальные параметры токсикометрии
Изучение любых вредных веществ предусматривает установление количественных показателей токсичности и опасности его, т.е. параметров токсикометрии.
Токсикометрия – совокупность методов и приемов исследований для количественной оценки токсичности и опасности ядов.
Опасность вещества – это вероятность возникновения неприятных для здоровья эффектов в реальных условиях производства или применения химических соединений.
Первичные (экспериментальные) и вторичные (производные) параметры токсикометрии.
Параметры токсикометрии, которые определяются непосредственно в эксперименте, называются экспериментальными.
В качестве экспериментальных параметров используются следующие:
СL50 – концентрация средняя смертельная – вызывает гибель 50 % подопытных животных (мыши, крысы) при ингаляционном воздействии в течение двух и четырех часов и последующем 14-дневном сроке наблюдения (мг/кг).
DL50 – доза средняя смертельная – вызывает гибель 50% подопытных животных при однократном введении в желудок, брюшную полость с последующим 14-дневным сроком наблюдения (мг/кг).
DL0 (CL0) – доза максимально переносимая – наибольшее количество вредного вещества, введение которого в организм не вызывает гибели животных.
DL100 (CL100) – доза абсолютно смертельная – наименьшее количество вредного вещества, вызывающее гибель 100 % подопытных животных.
Limac int – порог острого интегрального действия – минимальная доза, вызывающая изменение биологических показателей на уровне целостного организма, которые выходят за пределы приспособительных физиологических реакций.
Limfcsp – порог острого избирательного действия – минимальная доза, вызывающая изменение биологических функций отдельных органов и систем организма.
Limohint – порог общетоксического хронического действия – минимальная доза вещества, при воздействии которой в течение четырех часов по пять раз в неделю на протяжении не менее четырех месяцев возникают изменения, выходящие за пределы физиологических приспособительных реакций.
Limch cp – порог отдаленных последствий – минимальная доза вещества, вызывающая изменение отдельных органов и систем организма, которые выходят за пределы приспособительных физиологических реакций в условиях хронического воздействия.
Наиболее статически значимыми в характеристике токсичности ядов по смертельному эффекту являются параметры CL50 и DL50.
Пороговая концентрация яда в крови – это параметр, который можно оценить при первых симптомах отравления.
Критическая концентрация – это параметр клинической токсикометрии, соответствующий развернутой клинической картине отравления.
Степень токсичности – величина, обратная средней смертной дозе.
Одним из ведущих факторов, обусловливающих развитие хронического отравления, является процесс кумуляции.
Количественная оценка кумулятивных свойств вредных веществ в промышленной осуществляется по величине коэффициента кумуляции.
Коэффициент кумуляции – отношение суммарной дозы яда, вызывающего стремительный эффект у 50 % подопытных животных при многократном пробном введении, к величине дозы, вызывающей тот же эффект при однократном введении:
Слгд = DL50(n) /DL50 ,
где DL50 (n) – суммарная средняя смертельная доза при n – кратном воздействии. Этот коэффициент – величина, обратная интенсивности кумуляции. Величина коэффициента кумуляции менее 1 свидетельствует о способности вещества к сверхкумуляции; от 1 до 3 – о выраженной кумуляции, от 3 до 5 – о средней кумуляции, более 5 о слабой способности к кумуляции.
Производные параметры токсикометрии
Полученные в острых опытах параметры токсичности (CL50, Limac inf, Limzcsp) позволяют рассчитывать зоны острого, хронического и специфического действия, которые дают возможность оценить опасность вещества.
Опасность оценивается двумя группами количественных показателей:
- критерием потенциальной опасности;
- критерием реальной опасности.
Потенциальная опасность определяется коэффициентом возможного ингаляционного отравления:
КВИО = С20/СL50 ,
где С20 – насыщенная концентрация вредных веществ в воздухе при Т = 20 °С, мг/м3.
Чем выше насыщенная концентрация вещества при комнатной температуре и ниже средняя смертельная концентрация (знач. КВИО больше), тем вероятнее возможность развития острого отравления. Это одна из основных закономерностей токсикометрии.
Анализ оценки опасностей различных промышленных ядов по величине КВИО показывает, что в ряде случаев малотоксичное, но высоколетучее вещество в условиях производства может оказаться более опасным в плане развития острого отравления, чем высокотоксичное, но малолетучее соединение.
О реальной опасности развития острого отравления можно судить по величине зоны острого действия.
Зона острого действия (Zас) – это отношение средней смертельной концентрации CL50 к пороговой концентрации Limac при однократном воздействии:
Zас = CL50 / Limac.
Она является показателем компенсаторных свойств организма, его способности к обезвреживанию и выведению из организма ядов и компенсации поврежденных функций. Чем меньше Zac, тем больше опасность острого отравления.
Показателями реальной опасности развития хронической интоксикации являются значения зон хронического и биологического действия.
Зона хронического действия (Zch) – отношение пороговой концентрации при однократном воздействии Limac к пороговой концентрации при хроническом воздействии Limch:
Zch = Limac / Limch.
Величина Zch используется для характеристики опасности яда при хроническом воздействии. Опасность хронического отравления прямо пропорциональна величине Zch.
Зона хронического действия является показателем компенсаторных свойств организма на низкомолекулярном уровне.
Зона биологического действия (Zbiol) – соотношение средней смертной концентрации CL50 к пороговой концентрации при хроническом воздействии Limch:
Zbiol = CL50 / Limch.
Чем больше значение Zbiol , тем выраженнее способность соединения к кумуляции в организме.
После определения параметров токсикометрии проводят обоснование коэффициента запаса. Величина его зависит от особенностей яда, адекватности и чувствительности показателей при определении Limch и пр. В обычных условиях коэффициент принимается в интервалах от 3 до 20. Величина коэффициента запаса возрастает при следующих обстоятельствах:
- увеличении абсолютной токсичности;
- увеличении КВИО;
- уменьшении зоны острого действия;
- увеличении кумулятивных свойств;
- существенных (более 3 раз) различиях в видовой чувствительности;
- выраженном кожно-резорбтивном действии.
Межвидовые различия в чувствительности подопытных животных оцениваются по отношению DL50 для наиболее устойчивого вида животных к DL50 для наименее чувствительного при одном и том же пути введения в организм.
Имея коэффициенты запаса, рассчитывают предельно допустимую концентрацию вредного вещества:
ПДК = Limch × k,
где к – коэффициент запаса.
Соотношение между основными и производными параметрами токсикометрии представлено на схеме 1.
Схема 3

Классификация вредных веществ по степени опасности
Параметры токсикометрии лежат в основе классификации вредных веществ по степени опасности.
Принадлежность химических веществ к соответствующему классу опасности определяется величинами семи показателей (табл. 2).
Таблица 2
Классификация ядов по степени опасности
|
Показатель |
Класс опасности |
|||
|
1 |
2 |
3 |
4 |
|
|
ПДК вредных веществ в воздухе рабочей зоны, мг/м3 |
менее 0,1 |
0,1-1,0 |
1,0-10 |
более 10 |
|
Смертельная (средняя) доза при введении в желудок DL50, м/кг |
менее 15 |
15-150 |
151-5000 |
более 5000 |
|
Средняя смертельная доза при нанесении на кожу DL50, мг/кг |
менее 100 |
100-500 |
501-2500 |
более 2500 |
|
Средняя смертельная концентрация в воздухе CL50, мг/м3 |
менее 500 |
500-5000 |
5001-50000 |
более 50000 |
|
Зона острого действия Zас |
менее 6 |
6-18 |
18,1-59 |
более 54 |
|
Зона хронических действий Zch |
более 10 |
10-5 |
4,9-2,5 |
менее 2,5 |
|
КВИО |
более 300 |
300-30 |
29-3 |
менее 3,0 |
Классификация вредных веществ по степени опасности
При определении класса опасности веществ определяющим является тот показатель, который свидетельствует о наибольшей степени опасности.
Классификация не распространяется на пестициды. Классификация пестицидов по степени опасности предложена Всемирной организацией здравоохранения (ВОЗ) в 1979 г.
Классификация пестицидов по степени опасности, предложенная ВОЗ
Критерии токсичности используются для гигиенической классификации пестицидов и по другим признакам.
По степени кожно-резорбтивной токсичности и величине кожно-орального коэффициента, определяемого по величине отношения DL50 при накожном нанесении к величине DL50 при введении внутрь, все пестициды подразделяют на 3 группы:
- резковыраженная (DL50 < 50 мг/кг, кожно-оральный коэффициент
меньше 3).
- выраженная (DL50 от 50 до 2000 мг/кг, кожно-оральный коэффициент от 3
до 10).
- слабовыраженная (DL50 > 2000 мг/кг, кожно-оральный коэффициент > 10).
Методы определения параметров токсикометрии
В зависимости от цели токсикометрические исследования проводятся по-разному. Но для решения задач гигиенической регламентации методические приемы, условия проведения и оценка результатов унифицированы.
Исследование токсичности веществ начинается с изучения смертельных эффектов в острых опытах. Проникновение веществ в организм осуществляется при вдыхании, введении в желудок, нанесении на кожные покровы и слизистые оболочки.
Каждый путь поступления соединений в организм требует определенных условий.
При оценке степени токсичности при энтеральном пути поступления наиболее часто вещество вводится непосредственно в желудок с помощью металлических или пластмассовых зондов. Введение соединений проводится через 3 часа после кормления, вводимый объем не должен превышать для мышей – 1 мл, для крыс – 5 мл.
Кормление животных осуществляется через 3 часа после введения вещества. Изучаемое соединение вводится в чистом виде. Если это невозможно, то используют растворители. Обычно такие вещества вводят в водных растворах, плохо растворимые соединения – в растительном масле или в виде суспензии в 1-2-процентном растворе крахмала. Следует помнить, что острая токсичность может существенно меняться в зависимости от используемого растворителя. Поэтому используемый растворитель обязательно вводится контрольной группе животных. Поступление вредных химических веществ через дыхательные пути в производственных условиях играет ведущую роль в возникновении профессиональных заболеваний (отравлений). В лабораторных условиях используются два способа ингаляционного воздействия на лабораторных животных химическими веществами:
1. Статистический способ используется для ориентированных оценок степени токсичности летучих веществ при создании постоянной концентрации в замкнутом пространстве (специальных камерах и эксикаторах).
2. Динамический способ позволяет обеспечивать непрерывную подачу вещества в камеру, что создает условия для поддержания концентрации соединения в относительно постоянном уровне и обеспечивает необходимый воздухообмен.
Наряду с определением параметров токсикометрии смертельного уровня большое прикладное значение имеют параметры острой токсичности, как пороги вредного воздействия при неоднократном поступлении по интегральным (неспецифическим) и специфическим показателям (Limfc int и Limfc sp).
Определение порога острого действия при однократном воздействии по применению интегральных показателей проводится с использованием не менее 3-х концентраций.
Оценка функционального состояния экспериментальных животных проводится через 4 часа после затравки, а затем на 2-й, 4-й и 8-й дни опыта. При этом учитываются максимальные отклонения величины исследуемого показателя. Определение порога вредного действия по большинству специфических показателей регламентируется методическими показаниями, утвержденными Минздравом России.
Исследование местного раздражающего действия при аппликации на кожу проводится на двух видах экспериментальных животных.
Количество животных – не менее 10 особей в группе. Участок аппликации составляет для кроликов 7х9 см, для морских свинок 5х5 см. За два дня до эксперимента тщательно выстригают участки шерсти по обе стороны от позвоночника. На время эксперимента животных фиксируют. Время экспозиции – 4 часа. Исследуемое вещество наносится из расчета 20 мг/см2. Оставшееся после окончания эксперимента вещество удаляется теплой водой с мылом. Реакцию кожи регистрируют через 1 и 15 часов после однократной аппликации. Степень выраженности раздражающего действия вещества на кожные покровы определяют по классификации (11 классов): 0 – отсутствие действия; 10 – растворы вещества вызывают некроз.
Исследование местного действия вещества на слизистую оболочку глаза проводится при закапывании в конъюнктивный мешок одной капли соединения. В дальнейшем в течение двух часов наблюдают за прозрачностью роговицы и слизистой оболочки. Развитие помутнения роговицы, острое воспаление слизистой оболочки с последующим рубцеванием век свидетельствует о наличии у вещества резко выраженного раздражающего эффекта.
Для переноса результатов экспериментальных токсических опытов с животных на человека существуют правило экстраполяции: если смертельная доза для четырех типов животных (мыши, крысы, морские свинки, кролики) различаются незначительно (менее чем в три раза), то существует высокая вероятность (свыше 70 %), что для человека они будут такими же.
Существуют следующие коэффициенты пересчета:
с крысы – 5,9;
с морской свинки – 4,7;
с кролика – 3,2;
с мыши – 11,8.
В настоящее время в токсикологии принято несколько методов оценки кумуляции. С помощью метода, предложенного Каганом, животным ежедневно вводят вещество в долях от установленной DL50 (1/5, 1/10, 1/20). Данный метод позволяет прогнозировать опасность развития хронического отравления. Опыт по развернутой схеме продолжается четыре месяца.
Санитарно-гигиеническое нормирование вредных веществ
Санитарно-гигиеническое нормирование – это деятельность по установлению нормативов предельно допустимых воздействий человека на природу. Под воздействием понимается антропогенная деятельность, связанная с экономическими, культурными и другими интересами человека и вносящая изменения в природную среду.
Предельно допустимый уровень (ПДУ) – это уровень физического воздействия (шум, тепловое, световое, радиоактивное и т.д. излучение), которое при ежедневном воздействии в течение длительного времени на организм не вызывает патологических изменений или заболеваний, а также не нарушает нормальной деятельности человека.
Предельная допустимая концентрация (ПДК) – это максимальная концентрация вещества, которая, воздействуя на человека, не вызывает у него и его потомства биологических изменений, даже скрытых и временно компенсированных, в т.ч. изменений реактивности, адаптационно-компенсаторных возможностей, иммунологических реакций, нарушений физиологических циклов, а также других нарушений.
ПДК и ПДУ устанавливают для производств и окружающей среды. При их принятии руководствуются следующими принципами:
– приоритет медицинских и биологических показаний к установлению санитарных регламентов перед прочими подходами;
– пороговость действия неблагоприятных факторов (в том числе химических соединений с мутагенным или канцерогенным эффектом действия ионизирующего излучения);
– опережение разработки и внедрение профилактических мероприятий по сравнению с появлением опасного и вредного фактора.
Для ограничения воздействия вредных веществ применяют гигиеническое нормирование их содержания в различных средах. При установленном ПДК в воздухе рабочей зоны или в воздушном бассейне населенных пунктов ориентируются на токсикологический показатель или рефлекторную реакцию организма.
В связи с тем, что требование полного отсутствия промышленных ядов в зоне дыхания работающих часто невыполнимо, особую значимость приобретает гигиеническая регламентация содержания вредных веществ в воздухе рабочей зоны. Такая регламентация осуществляется в три этапа:
1. обоснование ориентировочно безопасного уровня воздействия (ОБУВ);
2. обоснование ПДК;
3. корректировка ПДК с учетом условий труда работающих и состояния их здоровья.
ОБУВ устанавливается временно – на период, предшествующий проектированию производства. Значение ОБУВ определяется путем расчета по физическим или химическим свойствам или путем гентерполяций и экстраполяции в гомологических рядах соединений, либо по показателям острой токсичности. ОБУВ должны пересматриваться через два года после их утверждения. ОБУВ не устанавливаются:
- для веществ, опасных в плане развития отдаленных и необратимых эффектов;
- для веществ, подлежащих широкому внедрению в практику.
Для санитарной оценки воздушной среды используются следующие показатели: ПДКр.з. – ПДК вредного вещества в воздухе рабочей зоны, мг/м3. Эта концентрация не должна вызывать у работающих при ежедневном вдыхании в пределах 8 часов в течение всего рабочего стажа заболеваний или отклонений в состоянии здоровья. Рабочей зоной считается пространство высотой до 2 м над уровнем пола или площадки, на которой находятся места постоянного или временного пребывания рабочих.
До недавнего времени ПДК химических веществ оценивали как максимально разовые. Превышение их даже в течение короткого времени запрещалось. В последнее время для веществ, обладающих кумулятивными свойствами, введена вторая величина – среднесменная концентрация. Это средняя концентрация, полученная путем непрерывного или прерывного отбора проб воздуха при суммарном времени не менее 75 % продолжительности рабочей смены.
Содержание вредных веществ в атмосферном воздухе населенных пунктов также регламентируется ПДК, при этом нормируется среднесуточная и максимально разовая величина. ПДК вредных веществ в воздухе населенных мест – это максимальные концентрации, отнесенные к определенному периоду осреднения (30 мин, 24 часа, 1 месяц, 1 год) и не оказывающие ни регламентированной вероятности их проявления, ни прямого, ни косвенно вредного воздействия на организм человека, включая отдаленные последствия для настоящего и последующего поколений, не снижающие работоспособность человека и не ухудшающие его самочувствия.
Для атмосферного воздуха ПДК ниже, чем для рабочей зоны.
Максимальная (разовая) концентрация ПДКМР – наиболее высокая из числа 30-минутных концентраций, зарегистрированных в данной точке за определенный период времени.
Среднесуточная концентрация ПДКСС – средняя из числа концентраций, выявленных в течение суток или отбираемых непрерывно в течение 24 ч.
Нормирование качества воды рек, озер и водохранилищ проводят в соответствии с «Санитарными правилами и нормами охраны поверхностных вод от загрязнений». При этом рассматриваются водоемы двух категорий: первая – хозяйственно-питьевого и культурно-бытового назначения, вторая – рыбно-хозяйственного назначения.
Лимитирующий признак вредности (ЛПВ) – признак вредного действия веществ, который характеризуется наименьшей пороговой концентрацией.
ЛПВ для водоемов хозяйственно-питьевого и культурно-бытового назначения используют трех видов: санитарно-токсикологический, общесанитарный и органолептический; для водоемов рыбохозяйственного назначения – еще два вида ЛПВ: токсикологический и рыбохозяйственный.
Санитарное состояние водоема отвечает требованиям норм при выполнении следующего соотношения:

где Сim – концентрация вещества первого ЛПВ в расчетном створе водоема.
Нормирование химического загрязнения почв осуществляется по предельно-допустимым концентрациям (ПДКn).
ПДКn – концентрация вещества (мг/кг) в пахотном слое почвы, которая не должна оказывать прямого или косвенного отрицательного влияния на соприкасающиеся с почвой среду и здоровье человека, а также на самоочищающую способность почвы.
По своей величине ПДКП значительно отличается от принятых допустимых концентраций для воды и воздуха.
Различают четыре разновидности ПДКП в зависимости от пути миграции веществ в сопредельные среды: ТВ – транслокационный показатель, характеризующий переход химического вещества из почвы через корневую систему в зеленую массу и плоды растений; МА – миграционный воздушный показатель, характеризующий переход химического вещества в атмосферу; МВ – миграционный водный показатель, характеризующий переход химического вещества из почвы в подземные грунтовые воды и водные источники; С – общесанитарный показатель, характеризующий влияние химического вещества на самоочищающую способность почвы и микробиоценоз.
В случае применения новых химических соединений, для которых отсутствуют ПДКП, рассчитывают временные допустимые концентрации:
ВДКП = 1,23 + 0,48 lg ПДКПр.
ПДКПр – ПДК для продуктов питания (овощных и плодовых культур), мг/кг.
Специфика, причины и механизм токсического действия
Понятие «химическая травма»
Острые отравления целесообразно рассматривать как химическую травму, развивающуюся вследствие введения в организм токсической дозы чужеродного химического вещества. Последствия, связанные со специфическим воздействием на организм токсического вещества, относятся к токсикогенному эффекту химической травмы. Он носит характер патогенной реакции и наиболее ярко проявляется в ранней стадии острых отравлений – токсикогенной, когда токсический агент находится в организме в дозе, способной оказывать специфическое действие. Одновременно могут включаться патологические процессы, лишенные «химической» специфичности.
Таким образом, общий токсический эффект является результатом специфического токсического действия и неспецифических реакций организма.
В токсикогенной фазе отравления выделяют два основных периода: период резорбции, продолжающийся до момента достижения максимальной концентрации токсичного вещества в крови, и период элиминации, от окончания момента резорбции до полного очищения крови от яда.
С точки зрения токсикодинамики специфическая симптоматика отравлений, отражающих «избирательную токсичность» ядов, наиболее ярко проявляется в токсикогенной фазе, особенно в период резорбции. Для последнего характерно формирование тяжело протекающих патологических синдромов острых отравлений, таких как экзотоксический шок, токсическая кома, асфиксия и др. В соматогенной фазе обычно развиваются патологические синдромы, лишенные выраженной токсической специфичности. Они трактуются как осложнения острых отравлений – это пневмония, острая почечная недостаточность, сепсис и др. Фазы и периоды отравлений представлены на схеме 2.
Фазы и периоды отравлений

Схема 2. Основные факторы, определяющие развитие острого отравления.
R – пространственный, С – концентрационный, t – временной.
Теория рецепторов токсичности
Представление о рецепторе как месте конкретного приложения и реализации токсичного действия яда до настоящего времени остается недостаточно ясным, несмотря на то, что эта идея была выдвинута Дж. Ленгли более ста двадцати лет назад.
Рецепторы (от лат. «rezeptiо» – принимать) – это органы или устройства, принимающие из внешней или внутренней среды организма и передающие их в центральную нервную систему. В токсикологическом понимании термин «рецептор» был предложен в начале 20-го века немецким ученым Эрлихом. Это получило научное обоснование после количественных исследований А. Кларка (1937 г.), показавшего, что между чужеродными веществами и их рецепторами возникает связь, по-видимому, аналогичная взаимодействию субстрата со специфическим ферментом.
Ферменты. Помимо тканевых белков в организме есть особые, специфические белки, называемые ферментами. Такие белки являются биологическими катализаторами, способными в очень высокой степени направлять, ускорять или замедлять химические процессы в организме и тем самым оказывать решающее влияние на жизненные процессы.
Ни один процесс в организме не обходится без ферментов. Они расщепляют сложные вещества пищевых продуктов на более простые и синтезируют из простых веществ необходимые для организма сложные соединения; участвуют в химических превращениях, обеспечивающих организм энергией; регулируют деятельность нервной системы и многое, многое другое. В живом организме имеется свыше тысячи различных ферментов.
Характерной особенностью ферментов является специфичность их действия; каждому типу химических превращений соответствует свой наиболее активный вид фермента. Некоторые ферменты имеют широкий диапазон действия, область действия других ограничена активным участием в каком-нибудь одном превращении. Например, очень важную роль в деятельности нервной системы играет особое вещество – ацетилхолин. Оказалось, что это вещество образуется только при помощи фермента холинацетилазы, а разрушение ацетилхолина происходит при обязательном участии фермента холинэстеразы.
Несмотря на столь важное значение ферментов для деятельности организма, количественное содержание каждого из них чрезвычайно мало по сравнению с количеством белков, входящих в состав тканей. Естественно, что только благодаря очень высокой производительности этих небольших количеств ферментов обеспечивается нормальное существование живых организмов. Фермент пепсин, к примеру, за 1,5-2 ч. в мягких условиях организма расщепляет яичный белок, чего нельзя достигнуть без фермента за такой короткий срок даже при помощи самых активных химических реагентов; известно также, что одна молекула холинэстеразы за 1 сек. расщепляет примерно 10000 молекул ацетилхолина.
В живом организме деятельность всех ферментов строго согласована и координирована, тем самым обеспечивается существование белковых тел и непрерывный обмен с окружающей средой; нарушение нормальной деятельности ферментов приводит к заболеванию или гибели организма.
В состав любого фермента входит белок, обычно связанный с разнообразными соединениями небелкового характера – коферментами, которые придают всему ферменту высокую каталитическую и специфическую активность. В качестве коферментов могут быть некоторые биологически активные вещества (витамины, гормоны и др.), а также соединения различных металлов.
Каждый фермент имеет определенный объем и определенную поверхность, образованную полипептидными цепями белка. Рельеф поверхности фермента может иметь самые причудливые очертания, определяемые первичной, вторичной и третичной структурами белка, а также функциональными группами аминокислот. В химическом отношении эта поверхность неоднородна и на ней обычно имеется только небольшой участок, так называемый активный центр, ответственный за деятельность фермента. Все химические превращения в организме протекают на поверхности фермента, причем решающее значение имеет активный центр.
Очевидно, что специфическое действие фермента, выступающего при этом в качестве реагента, только на вполне определенные вещества (субстраты) и на вполне определенный тип химических превращений связано с более или менее полным соответствием структуры активного центра фермента со структурой субстрата. Чем больше соответствуют эти структуры друг другу, тем ближе подходит субстрат к ферменту; при полном соответствии структур субстрат входит в фермент, как ключ в замок. При этом происходит активация субстрата, вследствие чего он легко подвергается химическим превращениям, быстро освобождая поверхность фермента.
На приведенном ниже рисунке изображена схема действия фермента
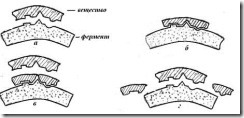
Рис.1. Схема взаимодействия фермента с веществом:
а - вещество и фермент удалены друг от друга; б - вещество подошло к ферменту; в - расщепление вещества на ферменте; г - остатки вещества при соответствии его структуры структуре субстрата.
Из этого рисунка можно уяснить и один из возможных вариантов нарушения деятельности ферментов. Например, какой-то другой субстрат, с другими свойствами, но обладающий сходной структурой, может присоединиться к ферменту таким образом, что частично или полностью закроет его активный центр и тем самым нарушит или совсем прекратит деятельность фермента (см. рисунок ниже). При этом "ложный" субстрат не подвергается никаким химическим превращениям и в то же время препятствует взаимодействию фермента с его естественным субстратом.
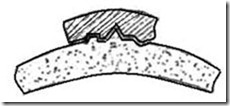
Рис. Блокировка фермента токсичным веществом
Вещество закрыло активную часть фермента, расщепление вещества не происходит.
Вещества, нарушающие нормальную деятельность ферментов, т.е. обладающие антиферментной активностью, называются ингибиторами.
Помимо такого, можно сказать, геометрического подобия структур фермента и субстрата существенное значение имеет и химическое строение активного центра. Высокая реакционная способность активного центра фермента, очевидно, связана с наличием в его структуре тех или иных функциональных группировок, принадлежащих аминокислотам полипептидной цепи, т.е. группировкам ОН, SН, NH2 ,СООН и т.д. При этом решающее значение имеет активация этих группировок, обусловленная влиянием соседних атомных групп и строением всего фермента в целом.
Как видно из приведенных примеров, большинство реакционноспособных группировок, входящих в активные центры ферментов, являются нуклеофильными. Поэтому такие группировки, а, следовательно, и ферменты в целом наиболее легко будут вступать в реакции нуклеофильного замещения и присоединения с веществами, химическая активность которых обусловлена наличием электрофильного центра, т.е. будут вступать во взаимодействие с электрофильными реагентами.
В соответствии с этим, антиферментной активностью могут обладать галоидированные соединения, производные кислот, соединения, имеющие в своем составе атомы с незаполненной электронной оболочкой, а также полярные молекулы, имеющие атомы с сильно пониженной электронной плотностью. При этом могут протекать процессы алкилирования, ацилирования и комплексообразования. В результате произойдет более или менее сильное нарушение структуры фермента и соответственно этому нарушение его функций, вплоть до полного их прекращения.
Поскольку нарушение функций ферментов приводит к нарушению деятельности организма, то вполне оправданным кажется представление о том, что токсическое действие отравляющих веществ связано с их определенно выраженным антиферментным действием.
Характер и степень токсического действия отравляющих веществ зависят в основном как от той роли, которую играют в организме поражаемые системы, так и от их способности легко и быстро реагировать с отравляющими веществами, образуя устойчивые соединения. Кроме того, важное значение имеют такие факторы, как восстановление активности ингибированного фермента (реактивация фермента) и скорость образования свежего фермента взамен потерявшего активность.
В процессе жизнедеятельности организма происходит непрерывное обновление белковых систем, в том числе и ферментов: разрушение старых, потерявших свою активность белков и образование взамен их новых, работоспособных белков той же структуры и того же назначения. В одних случаях эти процессы происходят медленно и не очень заметно, например отмирание старого рогового слоя кожи и образование нового, в других случаях быстро. Так, гемоглобин, содержащий в своей молекуле 300 аминокислот, образуется всего за 1,5 мин., а в каждую секунду разрушается и заново образуется 3 млн. эритроцитов (форменный элемент крови). Во всех этих и им подобных процессах ткани, клетки и образующийся белок ничем не отличаются от им подобных, как существовавших до них, так и существующих одновременно с ними.
Это постоянство строения и функций всех белковых систем обеспечивается аппаратом наследственности, управляющим процессами воспроизводства белков, клеток, тканей и всего организма в целом. Согласно современным представлениям ответственной за воспроизводство является клетка ткани.
Сама клетка является сложным образованием, состоящим из оболочки, плазмы и ядра с его оболочкой. В плазме клетки находятся субмикроскопические включения – рибосомы, митохондрии, лизосомы, так называемые органоиды.
Очень важную роль в созидательной деятельности клетки играют входящие в ее состав нуклеиновые кислоты (высокомолекулярные соединения небелкового характера), которые впервые были выделены из ядер клеток ("нуклеос" по-латыни – ядро, отсюда и название), хотя впоследствии они были найдены и в других частях клетки. Например, в настоящее время точно установлено, что синтез белка осуществляется в мельчайших образованиях или органоидах клетки при помощи различных нуклеиновых кислот и специфических ферментов.
При воспроизводстве белков, клеток, тканей и даже организма в целом возможны всякого рода нарушения работы аппарата наследственности, которые могут привести к тяжелым и даже гибельным для организма последствиям. Эти нарушения могут происходить под влиянием различных факторов, в том числе и под воздействием отравляющих веществ, которые могут либо умертвить клетку, либо затормозить некоторые ее функции, либо извратить созидательную деятельность клетки по синтезу белка, воздействуя на ее нуклеиновые кислоты. Во всех этих случаях отравляющие вещества являются клеточными ядами.
В связи с этим можно указать, что некоторые химические соединения изменяют состав нуклеиновых кислот, в результате чего нарушаются процессы воспроизводства и появляются мутации, в подавляющем числе случаев вредные для организма, нарушающие его нормальное функционирование. Степень нарушения функций или поражения организма зависит как от количества и роли претерпевших мутации белков систем, так и от скорости их образования.
Химические вещества, вызывающие мутации, называются мутагенными веществами, или хемомутантами. Естественно, что такие вещества являются в той или иной степени токсичными соединениями. В свою очередь многие отравляющие вещества – иприт, зарин и им подобные – также обладают мутагенным действием.
Обмен веществ
Хорошо известно, что многие заболевания связаны с нарушением обмена веществ.
Все вещества, принимающие участие в обмене, как поступающие в организм, так и образующиеся в нем, называются метаболитами, а сам обмен веществ иногда называют метаболизмом. Например, глюкоза после поступления в организм претерпевает целый ряд превращений с образованием уксусной, щавелевой, лимонной и других кислот (все они являются в этом случае метаболитами с вполне определенной ролью в процессе усвоения глюкозы).
Антиметаболитом называют всякое, обычно сходное с метаболитом соединение, которое включается вместо метаболита в обмен веществ и либо извращает этот обмен, либо прекращает его.
Принцип подмены метаболитов антиметаболитами широко используется в медицинской практике для борьбы с болезнетворными микробами. В частности, парааминобензойная кислота необходима для роста бактерий, а амид сульфаниловой кислоты (белый стрептоцид) и другие сульфамидные препараты являются ее антиметаболитами. Микроорганизмы поглощают вместо парааминобензойной кислоты сульфамидный препарат, который для них не является ростовым веществом, в результате чего рост и размножение бактерий прекращаются.
Среди отравляющих веществ известны также соединения, поражающее действие которых основано на подмене метаболитов. Например, фторуксусная кислота, которая включается вместо уксусной кислоты в цикл карбоновых кислот углеводного обмена (цикл Кребса); в результате этого в дальнейшем вместо лимонной кислоты (нормального продукта углеводного обмена) происходит образование ее антиметаболита – фторлимонной кислоты, на которой и обрывается весь цикл углеводного обмена.
На основании изложенного материала можно сделать вывод, что причины и механизмы токсического действия отравляющих веществ могут быть чрезвычайно разнообразны. В одних случаях токсические свойства обусловлены антиферментным действием отравляющих веществ, в других они связаны с мутагенной активностью, в третьих отравляющие вещества являются антиметаболитами. С другой стороны, физиологическая активность даже какого-либо одного отравляющего вещества может быть обусловлена одновременным действием рассмотренных ранее различных механизмов токсичности.
Кроме ферментов, рецепторами первичного действия ядов являются аминокислоты, нуклеиновые кислоты, пуриновые и пиримидиновые нуклеотиды, витамины. Рецепторами часто бывают наиболее реакционноспособные функциональные группы органических соединений, такие как сульфгидрильные, гидроксильные, карбоксильные, амин- и фосфорсодержащие, которые играют жизненно важную роль в метаболизме клетки. Наконец, в роли рецепторов токсичности выступают различные медиаторы и гормоны.
Таким образом, логичным является предположение известного токсиколога Э.Альберта, что любое химическое вещество, для того, чтобы производить биологическое действие, должно обладать, по крайней мере, двумя независимыми признаками:
1) сродством к рецепторам;
2) собственной физико-химической активностью.
Под сродством подразумевается степень связи вещества с рецептором, которая измеряется величиной, обратной скорости диссоциации комплекса «вещество + рецептор».
Как в свете этих данных выглядит характеристика токсичности? Наиболее элементарное представление о ней дает простая оккупационная теория Кларка, выдвинутая им для объяснения действия лекарств: токсическое действие вещества пропорционально площади рецепторов, занятой молекулами этого вещества. Максимальное токсическое действие вещества проявляется тогда, когда минимальное количество его молекул способно связывать и выводить из строя наиболее жизненно важные клетки – мишени. Дело не столько в количестве пораженных ядом рецепторов, сколько в их значимости для жизнедеятельности организма. Немаловажным является скорость образования комплексов ядов с рецепторами, их устойчивость и способность к обратной диссоциации, что нередко играет более важную роль, чем степень насыщения рецепторов ядов. Таким образом, современная теория рецепторов токсичности рассматривает комплекс «яд + рецептор» с точки зрения их взаимодействия. Считают, что ковалентные связи ядов с рецепторами прочны и труднообратимы. К счастью, количество токсичных веществ, способных образовывать ковалентные связи невелико. К ним относятся, например, препараты мышьяка, ртути и сурьмы. Большинство же известных в настоящее время токсичных веществ и лекарственных средств взаимодействует с рецептором за счет более лабильных, легко разрушающихся связей – ионных, водородных, ван-дер-ваальсовых, что дает возможность их успешного удаления из организма.
Плодотворной оказалась идея Эрлиха о существовании высокой специфичности первичной реакции взаимодействия яда и клетки, когда яд вмешивается в процессы обмена веществ благодаря своему структурному сходству с тем или иным метаболитом, медиатором, гормоном и т.д. Именно в этих случаях можно говорить о взаимодействии между ядом и рецептором как об отношении, напоминающем «ключ к замку» по Эрлиху. Эта идея послужила толчком к развитию химиотерапии, основанной на подборе лекарств по их избирательной точности для определенных структур организма, отличающихся специфическими, цитологическими и биохимическими признаками.
Однако в токсическом действии многих веществ отсутствует строгая избирательность. Их вмешательство в жизненные процессы основано не на специфических химических воздействиях с определенными клеточными рецепторами, а на взаимодействии со всей клеткой в целом. Этот принцип, вероятно, лежит в основе наркотического действия разнообразных органических и неорганических веществ, общим свойством которых является то, что они являются неэлектролитами. Для обозначения всех эффектов, которые прямо определяются физико-химическими свойствами вещества, предложен термин «неэлектролитное действие» (наркотическое, раздражающее, прижигающее, гемолитическое и др.). Такое действие иногда называют «физической» токсичностью.
Токсичное действие большинства веществ включает как неспецифические «физические», так и специфические «химические» компоненты и развивается по смешанному варианту.
Эти выводы весьма условны, т.к. они базируются на самых общих представлениях о механизме действия отравляющих веществ. Могут быть и другие механизмы токсичности, сведения о которых могут быть получены после тщательного изучения биохимии и физиологии живого организма.


