ТОКСИКОКИНЕТИКА
Токсикокинетика отвечает на вопрос: какова кинетика токсичного вещества в организме, т.е. рассматриваются пути поступления вредных веществ в организм, их транспорт и распределение, биотрансформация и выделение. Эти процессы протекают во времени с разной скоростью.
Свойства биологических мембран
Поступление чужеродных веществ в организм, их распределение между органами и тканями, биотрансформация (метаболизм) и выделение предполагают их проникновение (транспорт) через ряд биологических мембран.
Мембранные системы организма имеют одинаковое строение, но отличаются по функциональным свойствам. Они представляют подвижные структуры, образованные белково-фосфолипидными комплексами и обладающие ограниченной проницаемостью для различных соединений. В настоящее время за основу принимается гипотеза трехслойной мембраны.
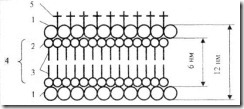
рис. Схема молекулярного строения биологической мембраны: 1 – молекулы белка; 2 – гидрофильная часть молекулы; 3 – углеродные цепи; 4 – двойной слой фосфолипидных молекул; 5 – олигосахариды.
Два белковых слоя, один из которых обращен в сторону цитоплазмы, а другой - наружу, заключают слой двойного липида. Снаружи липидных слоев с плавающими на них белками находится «карбогидратная шуба», состоящая из разных олигосахаридов, полимеров, включающих десятки типов моносахаридов, в том числе глюкозу. Одна из предполагаемых функций этой «шубы» заключается в том, что она способна отличать клетки собственного организма от других. Двойной липидный слой составляет структурный каркас мембраны. Молекулы фосфолипида ориентированы таким образом, что их гидрофильные группы направлены в стороны белка, а гидрофобные поверхности соприкасаются. Толщина каждого слоя 2-4 нм. Предполагают, что в клеточных мембранах существуют ультрамикроскопические поры, образованные гидрофильным веществом, причем мембраны и поры имеют определенные электрические заряды. На мембране и внутри ее могут располагаться системы ферментов, состоящих из белковых молекул.
Белки, связанные только с поверхностью мембраны, называют «внешними».
Белки, которые проникают внутрь, называют «внутренними». Мембрана – нестатичная структура. Соотношение липидов и белков в ней легко изменяется в соответствии с функциональными потребностями.
Изучение функции клеточных и внутриклеточных мембран позволило выделить специальную группу веществ, оказывающих специфическое мембранотоксическое действие, так называемые мембранотоксины. К их числу относят экзогенные и эндогенные вещества, обладающие фосфолипазной активностью, в результате которой происходит дезорганизация и разрушение основной жидкокристаллической структуры мембран с последующей гибелью клеток. Однако обнаружены и некоторые соединения, способствующие стабилизации мембран (холестерин, кортизон, аминозин, салицилаты).
Повреждение мембранных структур клеток является одной из основных причин нарушения их жизнедеятельности. Существует несколько механизмов повреждения мембран. Наиболее существенны четыре:
• ионами кальция;
• перекисным окислением, активируемым ионами Fe2+;
• ультрафиолетовым излучением и кислородом;
• механическим повреждением и разрушающим действием антител.
При острых отравлениях наиболее распространенной причиной повреждения является перекисное окисление липидов в мембранах митохондрий, в результате чего происходит увеличение проницаемости мембран для ионов, в первую очередь Н+ (или ОН-), затем К+, Na+, Ca2+. Следствием этого могут быть осмотические эффекты и разрывы мембран с выходом ферментов. Дальнейшее окисление мембран идет к полному их разрушению и гибели клеток.
Повреждение мембран при гипоксии, сопровождающее многие заболевания химической этиологии, связано с недостатком энергии, выделяющейся при метаболизме АТФ.
Таким образом, повреждение мембранных структур происходит по универсальным механизмам, которые приводят к изменению их проницаемости для ионов, что в свою очередь обусловлено изменением поверхностного заряда на мембране и изменением степени гидрофобности липидной фазы мембран. Оба этих фактора действуют одновременно, хотя их относительный вклад в итоговое изменение проницаемости в разных случаях различен. Эти же факторы определяют в конечном счете неспецифическое действие на проницаемость мембран различных соединений, например таких, как стероиды, белки и многие другие природные соединения. Процесс прохождения веществ через мембраны достаточно сложен, так как приходится учитывать не только функциональные особенности самих мембран, но и определенную роль протоплазмы и клеточных белков.
Мембрана – не просто пассивный барьер. Некоторые вещества проходят непосредственно через мембрану либо путем растворения в ней, либо путем химического взаимодействия с ее веществом.
Однако частично обмен осуществляется через поры. Они не обязательно являются каналами с фиксированным положением. Живая мембрана реагирует на изменяющиеся условия, открывая или закрывая определенные поры, что позволяет пропускать молекулы массой от 100 до 60 000.
Пути проникновения вредных веществ в организм человека
Токсические вещества, находящиеся в окружающей среде, могут проникать в организм человека несколькими путями:
· ингаляционным (через дыхательные пути);
· пероральным (через желудочно-кишечный тракт);
· перкутантным (через неповрежденную кожу).
· инъекционным.

Схема 3. Пути проникновения и выведения ядов в организм человека
Абсорбция через дыхательные пути
Абсорбция через дыхательные пути – основной путь поступления вредных веществ в организм человека на производстве. Ингаляционные отравления характеризуются наиболее быстрым поступлением яда в кровь.
Дыхательные пути являются идеальной системой для газообмена с поверхностью до 100 м2 при глубоком дыхании и сетью капилляров длиной около 2000 км. Их можно разделить на две части:
- верхние дыхательные пути: носоглотка и трахеобронхиальное дерево;
- нижняя часть, состоящая из бронхиол, ведущих в воздушные мешки (альвеолы), собранные в дольки.
Поведение газов и паров внутри дыхательных путей зависит от их растворимости и химической активности. Водорастворимые газы легко растворяются в воде, содержащейся в слизистой верхних дыхательных путей. Менее растворимые газы и пары достигают альвеол, в которых они абсорбируются и могут реагировать с эпителием, вызывая местные повреждения.
Жирорастворимые газы и пары диффундируют через неповрежденные альвеолярно-капиллярные мембраны. Скорость абсорбции зависит от их растворимости в крови, вентиляции, кровотока и интенсивности обмена веществ. Газообразные вещества, имеющие высокую растворимость, легко выделяются из легких с выдыхаемым воздухом.
Удержание частичек в дыхательных путях зависит от физических и химических свойств частичек, их размера и формы, а также от анатомических и патологических характеристик. Растворимые частички в дыхательных путях растворяются в зоне осаждения. Нерастворимые могут осаждаться тремя способами в зависимости от зоны осаждения:
- с помощью мукоцилиарного покрова как в верхних дыхательных путях, так и в нижней части дыхательных путей;
- в результате фагоцитоза (процесса захватывания бактерий особенными клетками – фагоцитами. Поглощенная частица переваривается или растворяется);
- путем прохождения непосредственно через альвеолярный эпителий.
Можно установить вполне определенную закономерность сорбции ядов через легкие для двух больших групп химических веществ.
Первая группа: нереагирующие пары и газы – в организме они не изменяются или их превращение происходит медленнее, чем накопление в крови. К ним относятся пары всех углеводородов ароматического и жирного ряда и их производных.
Вторая группа: реагирующие пары и газы – быстро растворяются в жидкости организма, легко вступают в химические реакции или претерпевают другие изменения, к ним относятся аммиак, сернистый газ, оксиды азота.
Нереагирующие пары и газы поступают в кровь на основе закона диффузии, т. е. вследствие разницы парциального давления газов и паров в альвеолярном воздухе и крови.
Вначале насыщение крови газами или парами вследствие большой разницы парциального давления происходит быстро, потом замедляется и, наконец, когда парциальное давление газов или паров в альвеолярном воздухе и крови уравняется, насыщение крови газами или парами прекращается.
Практический вывод: если при постоянной концентрации паров или газов в воздухе в течение очень короткого времени не наступило острое отравление, в дальнейшем оно не наступит.
Поглощение в желудочно-кишечном тракте (ЖКТ)
Поступление токсических веществ в ЖКТ происходит вместе с пищей и питьем в результате случайного попадания ядов в рот, а также путем заглатывания вдыхаемых нерастворимых частичек.
В быту пероральный путь поступления вредных веществ является основным, в производственных условиях он наблюдается сравнительно редко.
Классическим примером такого пути может служить поступление свинца. Это – мягкий металл, он легко стирается, загрязняет руки, не отмывается водой и при еде и курении может попасть в полость рта. Таким же путем могут попасть в организм кристаллические нитропроизводные бензола и его гомологов.
В ЖКТ условия всасывания ядов затруднены. Это объясняется тем, что ЖКТ имеет относительно небольшую поверхность, кроме того, при этом проявляется избирательный характер всасывания – легко всасываются вещества, хорошо растворимые в липидах. Кислая среда желудочного сока может изменить химические вещества в неблагоприятную для организма сторону. Так, соединения свинца, плохо растворимые в воде, хорошо растворяются в желудочном соке и поэтому легко всасываются.
На протяжении желудочно-кишечного тракта значительные градиенты рН определяют различную скорость всасывания токсичных веществ. Кислотность желудочного сока близка к единице, вследствие чего все кислоты легко всасываются путем пассивной диффузии. Напротив, основания поступают из крови в желудок и отсюда в виде ионизированной формы движутся далее в кишечник.
В основном всасывание ядовитых веществ происходит в тонком кишечнике, секрет которого имеет рН 7,5-8,0. В кишечнике липидорастворимые вещества хорошо всасываются путем диффузии, а всасывание электролитов связано со степенью их ионизации. Трудно всасываются прочные комплексы токсичных веществ с белками.
На абсорбцию в ЖКТ оказывает влияние множество факторов:
- физико-химические свойства веществ, в особенности их растворимость и диссоциация;
- количество пищи в ЖКТ и перистальтика пищеварительного тракта;
- время нахождения пищи в разных отделах ЖКТ;
- свойства эпителия, его поверхность, рН, интенсивность кровообращения;
- гидротропизм, т. е. способность некоторых соединений преобразовывать нерастворимые соединения в более растворимые;
- присутствие других веществ, которые при реакции могут иметь синергетический или антагонистический эффект.
Большинство токсичных веществ, абсорбированных в ЖКТ, попадает в капилляры, затем в воротковую вену и по ней в печень. Здесь они изменяются в ходе обмена веществ и в большинстве случаев обезвреживаются. Кроме того, многочисленные токсические вещества, имеющиеся в крови после всасывания из ЖКТ, могут выделяться с желчью в кишечник.
Абсорбция через кожу
Кожа вместе со слизистой оболочкой естественных отверстий организма покрывает поверхность тела. Она представляет собой преграду для физических, химических и биологических агентов, сохраняет целостность организма и гомеостаз, выполняет другие физиологические функции.
Кожа состоит из трех слоев: эпидермиса, собственно кожи (дермы) и подкожной ткани (гиподермиса).
С точки зрения токсикологии наибольшее значение имеет эпидермис. Он состоит из многих слоев клеток. Под самым верхним слоем расположена липидная мембрана («барьерная»). Однако эта мембрана – несплошная: волосяные мешочки и протоки потовых желез проходят через нее и достигают дермы.
Существуют три пути проникновения токсичных веществ через кожу:
- через эпидермис;
- волосяные фолликулы;
- выводные протоки потовых желез.

рис.3. Схема поступления ядовитых веществ через кожу
Количество ядовитых веществ, которые могут проникнуть через кожу, находится в прямой зависимости от их растворимости в воде и липидах, величины поверхности соприкосновения с кожей и скорости протока в ней. Вещества с малым коэффициентом распределения неспособны вызвать отравления через кожу, так как быстро удаляются из организма через легкие.
Большое значение для поступления ядов через кожу имеет консистенция и летучесть вещества. Жидкие органические летучие вещества быстро испаряются с поверхности кожи и в организм не попадают. Летучие яды, входящие в состав мазей, паст, клеев, могут вызвать отравления через кожу.
Твердые и кристаллические органические вещества всасываются через кожу медленно и могут вызвать отравление. Наибольшую опасность представляют мало летучие вещества маслянистой консистенции (анилин, нитробензол). Они хорошо проникают через кожу и длительно задерживаются в ней.
Следует учитывать, что соли многих металлов, соединяясь с жирными кислотами и кожным салом, могут превращаться в жирорастворимые соединения и проникать через барьерный слой эпидермиса (особенно ртуть и таллий).
Механические повреждения кожи, термические и химические ожоги способствуют проникновению токсических веществ в организм.
Транспорт и распределение ядовитых веществ в организме
После поглощения любым путем вещества попадают в кровь, лимфу или какую-нибудь другую жидкость организма. Однако для большинства веществ наиболее важным средством транспортировки после всасывания является кровь. В крови вещества находятся либо в свободном состоянии, либо связаны каким -либо компонентом крови. Различные токсичные вещества и их метаболиты транспортируются кровью в разных формах. Вещества могут быть связаны с эритроцитами или с компонентами плазмы. Выраженное сродство к эритроцитам имеют немногие вещества. Оксид углерода связывается с гемом, а мышьяк – с глобином гемоглобина. Свинец на 96 % переносится эритроцитами. Ртуть, содержащаяся в органических соединениях, и цезий также связываются с эритроцитами, а неорганическая ртуть – с альбумином плазмы крови. Белки плазмы могут переносить вещества, растворимые в липидах. Органические кислоты образуют комплексы с различными веществами. К последним относятся щелочноземельные элементы, редкоземельные и некоторые тяжелые металлы, находящиеся в плазме в виде катионов. Обычно комплексы с органическими кислотами способны диффундировать и легко удаляются из тканей и органов.
Удаление токсичного вещества из крови зависит от его свойства связываться с компонентами крови. В некоторых случаях компоненты эритроцитов или плазмы могут удерживать яды продолжительное время. Таким образом, белки крови, способные связываться с токсичным веществом, помимо транспортной функции выполняют роль своеобразного защитного барьера.
Транспорт токсиканта через мембрану, не требующей затрат энергии и возможной в обоих направлений, как в клетку, так и из нее, называется простой диффузией. Транспорт токсиканта, проходящий против градиента концентрации (из области с меньшей концентраций в область с большей концентрации) называется активным транспортом.
Пинацитоз – это дополнительные транспортные процессы, предполагающие участие клеточной мембраны.
Распределение и кумуляция токсичных веществ в организме
Следующим этапом всасывания токсического вещества в кровь является его распределение в организме. Одним из основных показателей является объем распределения, т.е. характеристика пространства, в котором распределяется данное токсическое вещество. Существует три главных сектора распределения чужеродных веществ:
- внеклеточная жидкость (объем ее составляет примерно 14 л для человека массой 70 кг);
- внутриклеточная жидкость (объем примерно 28 л);
- жировая ткань (объем ее варьируется).
Накопление ксенобиотиков в отдельных частях организма называется депонированием.
Факторы, определяющие распределение ядов
Распределение токсичных веществ зависит от трех основных факторов: пространственного, временного и концентрационного.
Пространственный фактор определяет пути наружного поступления и распространение яда. Это распространение во многом связано с кровоснабжением органов и тканей. Наибольшее количество яда в единицу времени обычно поступает в легкие, почки, печень, головной мозг.
Под временным фактором подразумевается скорость поступления яда в организм и скорость выведения из организма, т.е. этот фактор отражает связь между временем действия яда и его токсического эффекта.
Концентрационный фактор – это концентрация яда в биологических средах, в частности в крови. Он считается основным в клинической токсикологии. Определение этого фактора позволяет различить токсикогенную и соматогенную фазу отравления и определить эффективность дезинтоксикационной терапии.
Объем растворения зависит от трех основных физико-химических свойств данного вещества: водорастворимости, жирорастворимости и способности к диссоциации. Водорастворимые соединения способны распространяться во всем водном секторе организма, жирорастворимые вещества депонируются преимущественно в липидах.
Отложение в жировых тканях
Жирорастворимые вещества проявляют большое сродство к тканям и органам, богатым липидами и жирами: жировой ткани, эндокринным железам, нервным волокнам. Многие из этих веществ могут накапливаться в жировой ткани.
Отложение в костной ткани
Многие вещества проявляют особое сродство к костной ткани: легкие и щелочноземельные элементы, некоторые коллоиды. Остеотропные вещества могут откладываться в минеральных компонентах кости с помощью двух основных механизмов:
- ионообмена катионов Са2+ из гидроксиапатита либо анионов с фосфатными анионами или анионами гидроксильной группы;
- абсорбции коллоидов на поверхности костных кристаллов.
Отложение в волосах и ногтях
Некоторые тяжелые металлы (свинец, цинк, кадмий, ртуть) проявляют сродство к SH-группам кератина, находящегося в волосах, и откладываются в них.
Процессы биотрансформации токсических веществ
Большинство чужеродных, органических, а также некоторые неорганические вещества, претерпевают в организме метаболические превращения благодаря катализу внутри- и внеклеточными ферментами. Эти реакции обычно приводят к образованию производных, молекулы которых более полярны, чем у исходных веществ, поэтому они легче выходят из организма.
Биотрансформация катализируется в соответствии с химической структурой чужеродного вещества ферментами, находящимися в различных компонентах клетки.
При биотрансформации, претерпеваемой чужеродными веществами в организме, могут быть выделены реакции двух типов:
- реакции фазы 1, в основном окисление, восстановление и гидролиз;
- реакции фазы 2, представляющие собой биосинтетические реакции конденсации, с помощью которых чужеродные вещества или их метаболиты, образующиеся по реакции фазы 1, соединяются с эндогенными субстратами.
Сами реакции фазы 1 разделены на два подкласса: катализируемые микросомными и немикросомными ферментами.
Реакции окисления, восстановления, гидролиза
Реакции окисления, катализируемые микросомными ферментами (микросомное окисление)
Окисление может быть представлено следующим образом:
RH + 2e- + 2H+ ® ROH + H2O.
чужеродное метаболит
вещество
Реакции окисления, катализируемые немикросомными ферментами (немикросомальное окисление)
Примером таких реакций может быть окисление спиртов через альдегиды до соответсвующих кислот. Окисление может катализироваться ферментами, присутствующими в митохондриях, растворимой фракции цитоплазмы или в плазме.
Понятие о летальном синтезе
Особенно важно для клинической токсикологии является изучение метаболических процессов, в ркезультате которых нетоксичное или малотоксичное вещество превращается в соединение более токсичное чем исходное. Это может осуществиться как в процессе разложения вещества, так и в процессе синтеза. Такое явление называется летальным синтезом.
Яркий пример такого превращения – метаболизм метилового спирта, токсичность которого полностью определяется продуктами его окисления: формальдегидом и муравьиной кислотой.
![]()
Метиловый спирт формальдегид муравьиная кислота
Метаболизм этилового спирта начинается с образовании ацетальдегида (уксусного альдегида), который в несколько раз токсичнее исходного продукта.
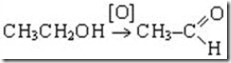 .
.
Этиловый спирт ацетальдегид
Тяжесть отравления этиленгликолем прямо пропорциональна степени окисления его до щавелевой кислоты.
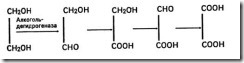
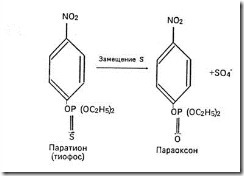
Еще один пример летального синтеза связан с метаболизмом известного инсектицида паратиона (тиофос). В этом случае происходит замещение атома серы на атом кислорода, в результате которого образуется параоксон – вещество более токсичное, чем тиофос.
Реакции восстановления, катализируемые микросомными ферментами (микросомальное восстановление)
В микросомальной фракции гепатоцитов содержатся ферменты, не только окисляющие, но и восстанавливающие чужеродные органические соединения.
Ароматические нитросоединения восстанавливаются в амины с промежуточным образованием гидроксиламинов с помощью микросомных ферментов.
Нитробензол восстанавливается таким образом в анилин. Процесс идет по схеме:
![]()
нитробензол нитрозобензол фенилгидроксил- анилин
амин
Немикросомальное восстановление
Реакции восстановления, катализированные немикросомальными ферментами включают:
- восстановление сульфидов в меркаптаны;
- восстановление гидроксамовых кислот в амиды;
- восстановление N-оксидов в амины;
- дегидроксилирование ароматических или алифатических гидроксилпроизводных.
Гидролиз, катализируемый микросомными и немикросомными ферментами
Эстеразы и амидазы, присутствующие в различных компонентах клетки и в плазме, катализируют гидролиз многих сложных эфиров и аминов. Алифатические нитрилы могут гидролизоваться с образованием кислот.
![]()
ацетонитрил уксусная аммиак
кислота
Одним из путей метаболизма токсичных веществ в организме является образование свободных радикалов. Образующийся свободный радикал может взаимодействовать с субклеточными структурами двумя путями: либо непосредственно повреждать ферментную систему, либо включать цепную реакцию переокисления липидов.
Биосинтетические реакции конденсации
Конденсация чужеродных веществ или их метаболитов с различными эндогенными субстратами обычно дает более полярные производные, которые легко выводятся из организма с мочой или желчью в виде конъюгатов. Конъюгация – это биосинтез при котором чужеродное вещество или его метаболит может соединяться с глюкуроновой кислотой, глицином, может сульфироваться, ацетилироваться или метилироваться. Таким образом, основными реакциями являются следующие:
- конденсация с глюкуроновой кислотой;
- сульфоконденсация;
- метилирование – метильная группа передается к аминопроизводному, фенолу или меркаптогруппе;
- конденсация с глицином;
- конденсация с глутатионом;
- конденсация с серой.
Различные метаболические превращения
Существуют такие метаболические превращения, которые не отнесены ни к одному из вышеуказанных классов. Одни и те же химические соединения могут претерпевать метаболические превращения как параллельно, так и последовательно. На метаболическую способность организма влияют генетические, физические, а также различные экзогенные факторы.
Пути выведения чужеродных веществ из организма
Экскреция – это выведение ядов с мочой, калом, потом, выдыхаемым воздухом во внешнюю среду.
Полное выведение яда из организма, включающее процессы биотрансформации и экскрецию, называется элиминацией.
Выделение токсичных веществ через почки происходит с помощью двух основных механизмов – пассивной диффузии и активного транспорта.
В результате пассивной фильтрации в почечных клубочках образуется ультрафильтрат, который содержит многие токсичные вещества, в том числе неэлектролиты, в той же концентрации, что и в плазме. Весь нефрон можно рассматривать как длинную полупроницаемую трубку, через стенки которой происходит диффузный обмен между протекающей кровью и формирующейся мочой. В почечных канальцах неэлектролиты, хорошо растворимые в жирах, путем пассивной диффузии могут проникать в двух направлениях: из канальцев в кровь и из крови в канальцы. Определяющим фактором почечного выделения является концентрационный индекс К, определяемый как
К = ![]() ,
,
где СМ – концентрация токсичного вещества в моче, СП – концентрация токсичного вещества в плазме. Значение К 1 – наоборот.
Направление пассивной диффузии органических веществ зависит от рН мочи: если канальцевая моча более щелочная, чем плазма, в мочу легко проникают слабые органические кислоты; если реакция мочи более кислая, в нее проходят слабые органические основания.
Кроме того, в почечных канальцах осуществляется активный транспорт сильных органических кислот и оснований эндогенного происхождения (например, мочевой кислоты, холина, гистамина и пр.), а также чужеродных соединений сходной с ними структуры с участием тех же переносчиков (например, чужеродных соединений, содержащих аминогруппу). Образующиеся в процессе метаболизма многих ядовитых веществ конъюгаты с глюкороновой, серной и другими кислотами также концентрируются в моче благодаря активному канальцевому транспорту.
Металлы выделяются преимущественно почками не только в свободном состоянии, если они циркулируют в виде ионов, но и в связанном, в виде органических комплексов, которые подвергаются клубочковой ультрафильтрации, а затем через канальцы проходят путем активного транспорта.
Выделение токсичных веществ, поступивших перорально, начинается уже в полости рта, где в слюне обнаруживаются многие электролиты, тяжелые металлы и т. д. Однако заглатывание слюны обычно способствует возвращению этих веществ в желудок.
Многие органические яды и образующиеся в печени их метаболиты с желчью поступают в кишечник, часть их выделяется из организма с калом, а часть повторно всасывается в кровь и выделяется с мочой. Возможен еще более сложный путь, обнаруженный у морфина, когда из кишечника чужеродное вещество попадает в кровь и снова возвращается в печень (внутрипеченочная циркуляция яда).
Большинство металлов, задерживающихся в печени, может связываться с желчными кислотами (марганец) и с желчью выделяться через кишечник. При этом большую роль играет форма, в которой данный металл депонируется в тканях. Например, металлы в коллоидном состоянии длительно остаются в печени и выделяются преимущественно с калом.
Таким образом, удалению через кишечник с калом подвергаются:
1) вещества, не всосавшиеся в кровь при их пероральном поступлении;
2) вещества, выделенные с желчью из печени;
3) вещества, поступившие в кишечник через мембраны его стенки.
Большинство летучих ядов выделяется из организма в основном в неизменном виде с выдыхаемом воздухом. Начальная скорость выделения через легкие газов и паров определяется их физико-химическими свойствами: чем меньше коэффициент растворимости в воде, тем быстрее происходит их выделение, особенно той части, которая находится в циркулирующей крови. Выделение их фракции, депонированной в жировой ткани, задерживается и происходит гораздо медленнее, тем более, что это количество может быть очень значительным, так как жировая ткань может составить более 20 % от общей массы человека. Например, около 50 % поступившего ингаляционным путем хлороформа выделяется в течение первых 8-12 часов, а остальная часть – во второй фазе выделения, которая продолжается несколько суток.
Многие токсичные вещества, подвергаясь медленной биотрансформации в организме, выделяются в виде основных продуктов распада: воды и углекислоты, которая выходит с выдыхаемым воздухом. Последняя образуется при метаболизме многих органических соединений, в том числе бензола, стирола, четыреххлористого углерода, метилового спирта, этиленгликоля, ацетона и пр.
Через кожу, в частности, с потом выходят из организма многие вещества, например, этиловый спирт, ацетон, фенолы, хлорированные углеводороды и пр. Однако за редким исключением (например, концентрация сероуглерода в поте в несколько раз выше, чем в моче), общее количество удаляемого таким образом токсичного вещества невелико и не играет существенной роли.
При кормлении грудью возникает опасность попадания с молоком некоторых жирорастворимых токсичных веществ в организм ребенка, в особенности пестицидов, органических растворителей и их метаболитов.
Виды возможного действия промышленных ядов
Все промышленные яды оказывают общее действие на организм. При этом для ряда токсичных веществ характерно преимущественное действие в точках своего приложения (кислоты, щелочи), другие же оказывают резорбтивное действие, не вызывая поражения непосредственно на месте соприкосновения с тканями (тетраэтилсвинец).
Химические ожоги
Химические ожоги возникают при местном воздействии химически активных веществ на кожу, слизистую оболочку дыхательных путей и глаз. Степень ожога зависит от химической активности и токсичности вещества, его концентрации, температуры, продолжительности воздействия, а также от чувствительности пострадавшего.
Различают ожоги четырех степеней. Ожоги первой степени характеризуются покраснением, припухлостью кожи и болезненностью. При ожогах второй степени появляются пузыри, и возможно нагноение. При ожогах третьей степени, вследствие глубоких повреждений, возникают участки омертвления (некрозы) тканей. При ожогах четвертой степени поражаются не только вся толща кожи, но и глубоко лежащие ткани. Соляная, азотная, серная и другие кислоты, хромовый ангидрид, а также концентрированные растворы щелочей (NaOH, KOH) NH4OH, попадая на кожу, вызывают химические ожоги, причем щелочные ожоги дают большую глубину поражения, что объясняется омылением щелочью жирового слоя кожи и растворением белковых веществ. Особенно опасно попадание кусочков твердой щелочи в глаза и на волосы (ожог глаз аммиаком и пероксидом водорода может привести к слепоте.)
При ожогах химическими веществами, способными прилипать к коже (горючие смолы, желтый фосфор), возникает еще и опасность общего отравления организма.
Избирательное действие ядов
Некоторые яды, кроме общего, оказывают избирательное действие по отношению к тем или иным органам или системам. Угарный газ, например, обладает высоким сродством к гемоглобину, образуя с ним карбоксигемоглобин (COHb). Марганец способен избирательно поражать нервную систему. Многие производственные яды способны вызвать аллергические реакции.
Поражение центральной нервной системы
Поражение центральной нервной и периферической системы проявляется нейротоксикацией и нейротоксикозами, что выражается совокупностью психических и соматовегетативных синдромов.
Изменение крови под действием промышленных ядов можно условно разделить на общие гематологические реакции и специфические изменения.
Гематологическое действие
Общие гематологические реакции возникают при острой интоксикации любым токсичным веществом независимо от механизмов его действия. Наиболее закономерными являются изменения со стороны белой крови: нейтрофильный лейкоцитоз со сдвигом влево, эозинопения, лимфопения, возрастание числа моноцитов.
Под специфическими изменениями крови следует понимать такие нарушения в ее составе, которые обусловлены действием определенного вредного фактора производственной среды (бензол, свинец и др.). При этом развиваются заболевания крови – лейкозы, анемия, нарушение свертываемости крови.
Поражение органов дыхания
Преимущественно поражение органов дыхания возникает при остром ингаляционном воздействии токсичных веществ раздражающего действия. При этом возможно развитие острого токсического бронхотрахеита, острого токсического бронхита, острого токсического отека легких, острой токсической пневмонии.
Поражение печени и мочевыделительной системы
Поражение печени и всей мочевыделительной системы происходит в результате воздействия веществ, которые можно выделить в группу гепатотропных ядов (хлороформ, четыреххлористый углерод). Под действием этих ядов развивается токсический гепатит.
Поражение мочевыделительной системы зависит от химического состава ядов, состояния почек и всего организма в целом. Одна группа веществ (металлы, их соединения, растворители, соединения мышьяка) вызывает токсические нефропатии. Другая группа веществ (ароматические амины) приводит к возникновению опухолей мочевыводящих путей.
Классификация факторов, определяющих развитие отравлений
Для определения токсического действия необходимо, чтобы токсичное вещество достигло рецепторов токсичности в достаточно большой дозе и в течение короткого времени.
Взаимодействие токсичного вещества с организмом зависит от многих факторов, относящихся к самому токсическому агенту, к конкретно сложившейся «токсической ситуации» и к пострадавшему человеку (табл. 3).
Таблица 3
Общая классификация факторов, определяющих развитие отравлений
|
I |
Основные факторы, относящиеся к ядам: - физико-химические свойства; - токсическая доза и концентрация в биосредах; - характер связи с рецепторами токсичности; - особенности распределения в биосредах; - степень химической чистоты и наличие примесей; - устойчивость и характер изменений при хранении. |
|
II |
Дополнительные факторы, относящиеся к конкретной «токсической ситуации»: - способ, вид и скорость поступления в организм; - возможность к кумуляции и привыкание к ядам; - совместное действие с другими токсичными веществами. |
|
III |
Основные факторы, характеризующие пострадавшего: - видовая чувствительность; - влияние массы тела, питания и физической нагрузки; - половая принадлежность; - возрастные особенности; - индивидуальная вариабельность и наследственность; - влияние биоритмов; - возможность развития аллергии и токсикомании; - общее состояние здоровья пострадавшего. |
|
IV |
Дополнительные факторы, влияющие на пострадавшего: - температура и влажность окружающего воздуха; - барометрическое давление; - шум и вибрация; - лучистая энергия и пр. |
Основными факторами следует считать определенные качества ядов и организма пострадавшего, а дополнительными - прочие факторы окружающей среды и конкретно сложившейся «токсической ситуации». С точки зрения решающего влияния на характер и выраженность отравлений, указанное разделение факторов на основные (внутренние) и дополнительные (внешние) является чисто условным, но необходимым. В самом деле, влияние дополнительных факторов редко может существенно изменить физико-химические свойства ядов и свойственную им токсичность, но, безусловно, сказывается на клинической картине отравления, его тяжести и последствиях.
Комбинированное действие ядов
В производственной и окружающей среде часто происходит комбиниро-ванное действие на организм двух или более ядов одновременно. Очень часты комбинации оксида углерода и диоксида серы при взрывных работах; паров бензола, нитробензола и оксидов азота в производстве нитробензола; паров бензола, толуола, ксилола, сероуглерода в коксохимическом производстве. Постоянное применение лекарственных препаратов является дополнительным фактором, который может оказывать влияние на токсикодинамику и токсикокинетику различных промышленных химических соединений в организме людей, подвергающихся их воздействию.
Наличие двух или нескольких чужеродных веществ в организме может приводить к изменениям в абсорбции, транспорте, распределении, кумуляции, обмене веществ и выделении каждого из них. Поэтому во всех случаях, когда проводится оценка воздействия химических соединений на рабочих, необходимо учитывать комбинированное воздействие и принимать во внимание его последствия.
Комбинированное действие вредных веществ – это одновременное или последовательное действие на организм нескольких ядов при одном и том же пути поступления.
Различают несколько видов комбинированного действия ядов.
1. Аддитивное действие – феномен суммированных эффектов. При этом суммарный эффект равен сумме эффектов действующих компонентов. Аддитивность характерна для веществ однонаправленного действия, когда компоненты смеси оказывают влияние на одни и те же системы организма, причем при количественно одинаковой замене компонентов друг другом токсичность смеси не меняется. Если в воздухе присутствуют пары двух раздражающих веществ, для которых установлена ПДК = 10 мг/м3 для каждого, то это значит, что в комбинации они окажут такое же действие, как концентрация 20 мг/м3 какого-либо одного из этих веществ.
Имеющиеся данные свидетельствуют о том, что в большинстве случаев производственные яды в сочетании действуют по типу суммации.
2. Потенцированное действие (синергизм) – усиление эффекта. Компоненты смеси действуют при этом так, что одно вещество усиливает действие другого. Эффект комбинированного действия при синергизме больше аддитивного, и это учитывается при анализе гигиенической ситуации в конкретных производственных условиях.
3. Антагонистическое действие – такое действие, при котором эффект комбинированного действия менее ожидаемого. Компоненты смеси действуют так, что одно вещество ослабляет действие другого, эффект – менее аддитивного. Примером может служить антидотное взаимодействие между эзерином и атропином.
4. Независимое действие – комбинированный эффект не отличается от изолированного действия каждого яда в отдельности. Преобладает эффект наиболее токсичного вещества. Комбинации веществ с независимым действием встречаются достаточно часто, например бензол и раздражающие газы, смесь продуктов сгорания и пыли.
Наряду с комбинированным влиянием ядов возможно их комплексное действие, когда яды поступают в организм одновременно, но разными путями (через органы дыхания и ЖКТ, органы дыхания и кожу и т. д.).
Взаимосвязь состава и строения веществ с их токсичностью
История раскрытия связей между химической структурой веществ и их токсичностью насчитывает более ста лет. Изучение этих связей является одной из основных задач общей токсикологии как науки, имеющей профилактическое значение. Отметим основные моменты.
Влияние числа атомов углерода в молекуле вещества
По правилу Ричардсона, в гомологическом ряду сила наркотического действия неэлектролитов возрастает с увеличением числа атомов углерода в молекуле. Так, например, наркотическое действие усиливается от пентана (С5Н12) к октану (С8Н18), от метилового спирта (СН3ОН) к аллиловому (С4Н9СН2ОН).
Если принять силу наркотического действия этилового спирта за 1, то сила действия остальных выражается следующим образом: метиловый спирт (СН3ОН) – 0,8; пропиловый спирт (С2Н5СН2ОН) – 2; бутиловый спирт (С3Н7СН2ОН) – 3; аллиловый (С4Н9СН2ОН) – 4.
Однако правило Ричардсона имеет ряд исключений. Первые представители многих гомологических рядов – производные метана, обладают более сильным общим токсикологическим действием, чем последующие. Так, муравьиная кислота, формальдегид, метанол значительно токсичнее, чем соответственно уксусная кислота, ацетальдегид и этанол. Дальнейшее нарастание наркотического эффекта идет только для определенного ряда, а затем уменьшается, что связано с резким изменением растворимости.
Правило не действует также для углеводородов ароматического ряда.
С учетом этих исключений правило нарастания токсичности в гомологических рядах используется для предсказания токсичности новых веществ при помощи методов интерполяции и экстраполяции; оно может служить ориентиром для выбора в гомологическом ряду органического растворителя с меньшим наркотическим действием.
С усилением наркотического эффекта возрастает и гемолитическое действие веществ.
Правило разветвленных цепей
Важно также так называемое правило разветвленных цепей, согласно которому наркотическое действие ослабляется с разветвлением цепи углеродных атомов. Например, наркотическое действие изопентана (СН3)2СН(СН2)СН3 слабее
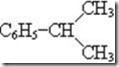 |
действия гептана СН3(СН2)5СН3, изопропилбензола слабее действия
пропил бензола С6Н5–СН2–СН2–СН3 и т.д. Установлено также, что углеводороды, имеющие одну длинную боковую цепь, оказывают большее наркотическое действие, чем их изомеры, имеющие несколько коротких боковых цепей. Замыкание цепи углеродных атомов усиливает наркотическое действие вещества.
Правило кратных связей
Биологическая активность вещества возрастает с увеличением кратности связей, т.е. с увеличением непредельности соединения (правило кратности связей). Наркотическое действие этана (СН3–СН3) слабее, чем этилена (СН2=СН2), а действие последнего слабее, чем ацетилена (СНºСН).
Непредельность вообще оказывает влияние на химическую активность. Так, например, с увеличением непредельности усиливаются раздражающие свойства веществ.
Влияние различных атомов и групп атомов на токсичность вещества
Введение в молекулу углеводорода атома кислорода усиливает наркотическое действие вещества: пропан (С3Н8) и даже пентан (С5Н12) – более слабые наркотики, чем ацетон (СН3СОСН3).
Резко меняется действие вещества при введении галогенов в молекулу углеводорода, в частности атома хлора. Известно, что с увеличением числа атомов хлора в гомологическом ряду возрастает наркотическое действие, например от метана (СН4) к хлороформу (СНСl3). Исключение составляет четыреххлористый углерод (ССl4), который обладает меньшим наркотическим действием, чем хлороформ.
Среди физиологически активных веществ видное место занимает группа соединений, содержащих в своем составе трихлорметильный фрагмент
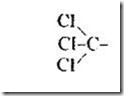
Как, правило, это вещества с высокой физиологической активностью разного спектра действия. Достаточно назвать такие препараты, как ДДТ (дихлордифенилтрихлорэтан) – один из самых эффективных инсектицидов, хлоральгидрат, который обладает снотворным действием сам и входит в состав некоторых снотворных препаратов, хлороформ, употребляемый в медицине для общего наркоза и т.д.
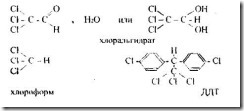
Хлорзамещенные углеводороды жирного ряда очень токсичны, вызывают жировое перерождение паренхиматозных органов. Такого же рода токсичностью обладают хлорзамещенные спирты, хлорпроизводные бензола. Эти же соединения вызывают значительные поражения нервной системы и оказывают сильное раздражающее действие.
ДДТ - Дихлордифенилтрихлорэтан

Применяется под названием ДДТ как инсектицид для борьбы с сельскохозяйственными вредителями, паразитами человека, комарами, мухами,
москитами и пр. Используется в виде дуста, в растворах (в керосине, веретенном масле, антраценовом масле и др.), в виде водных эмульсий или эмульсий с поверхностно-активными веществами, в виде аэрозолей в смеси с наполнителями. Технические названия применяемые препаратов: геразол, неоцид, ге-сарсол, гезонал, дуолит, хлорофенотан (последний препарат – смесь ДДТ с бензилбензоатом и этиламинобензоатом).
В промышленности ДДТ получается из этилового спирта, хлора и хлорбензола по схеме:
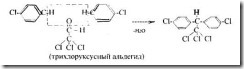
Физические свойства. В чистом виде – белые кристаллы. Т.пл. 108,5-109°С. Технический продукт плавится при 75-95°С. Практически не раств. в воде (раств. 0,2 части на миллион частей воды). Хорошо растворим в ацетоне, бензоле, эфире, диоксане, хлороформе, четыреххлористом углероде, пиридине.
Химические свойства. Термически устойчив. При действии едких щелочей отщепляет (в спиртовом растворе) НСl, образуя дихлордифенилди-хлорэтилен
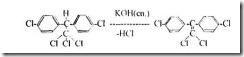
При нагревании с водно - спиртовыми щелочами образуется n,nf-дихлордифенилуксусная кислота. Отщепление НС1 от ДДТ происходит также при действии органических оснований, например, никотина.
Токсикологическое значение ДДТ определяется в первую очередь широким применением его в качестве контактного инсектицида против разнообразных насекомых.
Введенный внутрь ДДТ, особенно в виде раствора в масле, ядовит для всех теплокровных животных и человека. Является ядом центральной нервной системы. Вызывает патологические изменения в печени и почках животных. Тяжелые поражения наблюдаются в легких и трахее при введении препарата через органы дыхания. Смертельная доза ДДТ для человека не установлена.
Препарат, введенный в организм в масляных растворах, быстро всасывается и адсорбируется всеми органами, особенно костным мозгом, почками, мышцей языка, прямой кишкой, жировой тканью. Обладает кумулятивным действием. Задерживается в органах до 20 дней.
Из организма животных выделяется медленно и в основном через желудочно-кишечный тракт, а также молочными железами и почками. Конечный продукт превращения ДДТ в организме – дихлордифенилуксусная кислота (ДДУ), нетоксична для животных.
При использовании дихлордифенилтрихлорметилметана – ДДТ возникла настоящая экологическая проблема. Это вещество впервые было синтезировано и предложено в качестве средства борьбы с вредителями сельского хозяйства в 1940г. швейцарским химиком Паулем Мюллером, удостоенным за эту работу Нобелевской премии. Казалось, что применение этого вещества позволит человечеству справиться со многими проблемами – благодаря применению ДДТ резко уменьшился ущерб, наносимый саранчой и другими насекомыми – вредителями, миллионы людей были спасены от малярии, разносимой комарами. Однако вскоре изумление перед мощью ДДТ изменило радужную окраску на трагическую. Оказалось, что ДДТ вредно действует на все организмы, включая водоросли. Уже при содержании его несколько частей на миллиард падает скорость фотосинтеза, процесса, который является основным поставщиком кислорода в атмосферу. Далее выяснилось, что ДДТ, как и многие другие пестициды, обладает кумулятивным эффектом, вызывает тяжелые последствия – от токсических до мутагенных. Благодаря устойчивости ДДТ, он накапливается и передаётся по пищевым целям – от растений к травоядным животным, от них к хищникам, при этом в каждом последующем звене пищевой цепи содержание ДДТ увеличивается в 10 раз. В результате накопления препарата его концентрация в организме, который никогда не соприкасался с ядом, может достигнуть смертельных доз. Когда в США обнаружили, что в молоке кормящих матерей концентрация ДДТ превышает в четыре раза предельно допустимую дозу, применение его было запрещено. В 1970 году применение ДДТ запретили и в СССР. Однако в результате прежнего неограниченного применения ДДТ сегодня на Земле в биологическом круговороте находится около миллиона тонн этого препарата в силу чрезвычайно малой скорости его разложения (10 лет). Кроме того, в природной среде ДДТ способен превращаться в ещё более опасное соединение ДДЭ, поскольку последнее вещество еще медленнее, чем ДДТ метаболизируется и разрушается.
При рассмотрении вопроса о влиянии азота на характер химического соединения необходимо иметь в виду группу, в составе которой азот входит в ту или иную молекулу. Само собой разумеется, что азот в составе нитро- или нитрозогруппы резко отличается от азота в составе аминогруппы или какой-нибудь другой. Здесь рассматриваются следующие группы:
Нитрогруппа – NО2
Оксимная группа = NOH
Аминогруппа – NH2 или -NR2
Циангруппа – CN
Влияние нитрогруппы в молекуле о-нитробензилхлорида становится совершенно ясным при сравнении этого соединения с хлористым бензилом. Раздражающее действие последнего значительно слабее, чем у нитропроизводного. При рассмотрении других нитросоединений, обладающих слезоточивым действием, можно установить, как общее правило, что введение одной или нескольких нитрогрупп в соответствующую молекулу (особенно если последняя уже содержит галоид) приводит к усилению раздражающих свойств.
Представляет интерес в отношении связи структуры химического вещества и его биологического действия большая группа нитро- и аминопроизводных бензола и его гомологов.
Введение в молекулу бензола или толуола нитро- или аминогрупп (–NO2 или –NH2) резко меняет характер действия указанных веществ. На первое место выдвигается не наркотическое, а специфическое действие на кровь (образование метгемоглобина), на ЦНС. Увеличение в молекуле числа групп –NO2 придает веществу большую токсичность: нарастает кумулятивный эффект, возникает угнетение тканевого дыхания. Введением в нитросоединения бензола атома хлора резко увеличивается токсичность.
Наличие карбоксила или ацетилирование уменьшают токсичность соединения.
Влияние атома серы, в противоположность элементарным галогенам, физиологически относительно безвредно. На токсичность вещества в значительной мере влияет степень окисления серы в соединении. Так, b,b-дихлорэтилсульфид (соединение I) обладает кожно-нарывным действием.
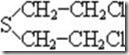 .
.
(I)
Если же окислить соединение до соответствующих сульфоксидов (соединение II) и сульфонов (соединение III), то токсичность этих соединений значительно снижается.
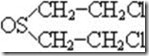 ;
; 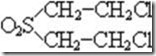 .
.
(II) (III)
Этот факт можно объяснить и понижением растворимости этих веществ в липидах.
Прогнозирование токсического действия неорганических соединений на основании их структуры и свойств представляет огромный интерес. Делаются попытки рассчитать токсичность ионов на основании таких показателей, как потенциал, атомный радиус, растворимость и т.д., и исследовать взаимосвязь между токсичностью ионов и положением металлов в периодической системе Д.И. Менделеева, а также между токсичностью и валентностью. Пока общих правил для определения токсического действия неорганических соединений установить не удалось.
Определенное влияние на токсическое действие веществ оказывает степень их химической чистоты и содержание примесей. Кроме того, при длительном хранении токсичность многих препаратов изменяется.
Математическая зависимость структура-токсичность
Уже в 1870 году была сформирована гипотеза, согласно которой ответная реакция биологической системы является функцией химической структуры вещества, которое на нее действует. Было показано, что зависимость «структура-токсичность» можно выразить математически с учетом изменений биологических ответных реакций при соответствующих небольших изменениях молекулярной структуры вещества. Количественные аспекты проблемы «структура-активность» были изучены в исследовании, проведенном в начале XX века Мейером и Овертоном. Согласно их данным, биологическая активность веществ с родственными структурами находится в линейной зависимости от липофильных свойств молекул. Было предложено использовать коэффициент распределения между липидной и водной фазами для описания наркотического действия молекул простых органических неэлектролитов.
Практически универсален метод, предложенный Хенчем (количественный многопараметровый подход к взаимоотношению «структура-активность»). Он основан на идее, что любой вид биологической активности в пределах ряда структурно-родственных химических соединений определяется суммой гидрофобных, электронных и стерических свойств молекул. Зависимость биологической активности веществ от их химической структуры может быть выражена уравнением:
lgC = K1(lgP)2 + K2(lg) + K3s + K4ES,
где C – молекулярная концентрация, вызывающая ответ определенной величины со стороны биологической системы; P – коэффициент распределения в системе октанол/вода; s - электронная константа Гаммета; ES - стерическая константа Тафта.
Цифровая константа s характеризует электронный эффект заместителя на ядро и реактивный центр молекулы. Стерическая константа ES представляет собой количественную меру общего пространственного эффекта заместителя на скорость химической реакции.
Связь между токсическим действием, электронными и стерическими константами можно объяснить тем, что биологическая активность в той или иной мере связана с химической активностью вещества, которая в свою очередь определяется электронными и пространственными свойствами молекулы, и поэтому может быть очень точно описана с помощью стерических и электронных констант. Для описания токсического действия не всегда требуется применять одновременно все компоненты модели Хэнча. Биологическое действие и токсичность некоторых генетических групп веществ можно определить с помощью одних лишь констант гидрофобности.
Уравнения, основанные на применении модели Хэнча, применимы для групп веществ со сходной структурой и не имеющих замещающих групп, отличающихся по структуре от исследованных веществ. Метод Хенча позволяет предсказывать фармацевтические, биоцидные и токсические эффекты органических соединений с большой точностью.
В последние годы модель Хенча и некоторые другие константы были использованы для описания токсического действия не только при однократном поступлении вещества в организм, но и в случаях, когда имеет место многократное, хроническое воздействие небольших доз. Эту модель также применяют для прогнозирования безопасных уровней содержания веществ в окружающей среде.
Кумуляция и адаптация к ядам
Хроническое действие яда наблюдается при разнообразных повторных его воздействиях. Оно может иметь место при повторных попаданиях яда в организм работающего как путем вдыхания паров или пыли, так и через кожу при контакте, например, с растворителями. Хроническое отравление тесно связано с кумуляцией в организме самого яда или вызванных им изменений. Слово «кумуляция» означает накопление. Этот термин взят из фармакологии, где им обозначают внезапное усиление действия некоторых лекарственных средств при длительном их применении. Накопление массы яда в организме называют материальной кумуляцией, а накопление вызванных ядом изменений – кумуляцией функциональной.
Свойство живого организма приспосабливаться к сдвигам в условиях существования путем изменения процессов жизнедеятельности называется адаптацией.
Процессом адаптации обозначается процесс, возникающий при воздействии любого фактора в силу его качественной или количественной необычности и выражающийся в адекватных этому воздействию изменениях в различных системах и на разных структурных уровнях. Способность к адаптации присуща всему живому. Адаптация может развиваться в течение очень разных периодов времени – от долей секунды до десятков лет.
Для обозначения приспособления организма к периодическому воздействию вредных веществ в условиях промышленного производства часто применяется термин «привыкание». Говоря о привыкании, обычно имеют в виду понижение чувствительности организма к химическому агенту, происходящее под влиянием повторного длительного воздействия яда. Привыкание может проявляться или ослаблением, или исчезновением неблагоприятных симптомов, появившихся в начале контакта с вредным веществом.
Для развития привыкания к хроническому воздействию яда необходимо, чтобы его концентрации (дозы) были достаточными для вызова ответной приспособительной реакции, но чтобы они не были чрезмерными, приводящими к быстрому и серьезному повреждению организма. При привыкании может иметь место не только восстановление нарушенных функций, но и восстановление измененных морфологических структур.
Необходимо отметить, что состояние организма при встрече с тем или иным фактором внешней среды играет существенную роль. Если воздействие является необычным только по своей интенсивности (например, углекислый газ в высоких концентрациях), то организм быстро пускает в ход уже существующие в нем адаптационные механизмы, адекватные действующему фактору. Однако в том случае, когда фактор является качественно новым и настолько интенсивно действующим, что требует новых приспособлений, повторяющееся воздействие будет способствовать выработке доминанты. Доминанта организует поиски адекватных механизмов адаптации. При повторных влияниях вырабатываются условные связи, пускающие в ход механизмы приспособления и компенсации раньше, чем успели произойти существенные сдвиги во внутренней среде организма. С течением времени работа сначала нервных центров, а затем и других систем организма, участвующих в этих процессах, тренируется, становится более слаженной, и весь механизм адаптации быстро пускается в ход под влиянием других сходных или даже необычных факторов.
Длительное воздействие малых доз или концентраций вредных химических агентов вызывает фазовые реакции большинства физиологических систем. Схематически реакцию организма на хроническое воздействие химического фактора при привыкании к нему можно разделить на три фазы: фазу первичных реакций, фазу развития привыкания, иногда с более или менее длительным устойчивым привыканием, и фазу срыва привыкания и выраженной интоксикации.
Фаза первичных реакций – это период поисков путей адаптации организма к изменившимся условиям внешней среды. В начальном периоде воздействия развивающиеся сдвиги непостоянны, обычно компенсируются и часто с трудом выявляются. Как правило, отсутствуют и изменения, характерные для специфического действия данного яда, но оказывается нарушенной стабильность функций ряда органов и систем, особенно регулирующих. Ранее всего возникают изменения функции и структуры щитовидной железы, которые затем нормализуются, причем, видимая нормализация одних показателей часто сопровождается изменениями других.
В фазе первичных реакций происходит функциональная активация систем, осуществляющих биотрансформацию яда, повышается активность симпатического отдела нервной системы, вместе с тем наблюдается снижение резистентности организма по отношению к экзогенным воздействиям. Первичная реакция отличается неустойчивостью, вариабельностью и практической невоспроизводимостью, границы их очень расплывчаты. В части случаев в этот период сдвиги вообще не обнаруживаются, они выявляются только при применении различных дополнительных, достаточно интенсивных воздействий. В эксперименте этот период длится относительно недолго (недели), а в жизни может растягиваться на несколько лет. При этом малая клиническая симптоматика сочетается с повышенной возбудимостью нервной системы, неустойчивостью нейрорегуляторных механизмов и часто – активизацией щитовидной железы.
Вторая фаза – развитие привыкания – характеризуется, как уже упоминалось, уменьшением реакции на воздействие (однако в течение этой фазы возможны и периоды снижения толерантности к токсическому агенту). Внешне – это фаза благополучия организма. Во время ее происходит тренировка наиболее адекватных, отобранных доминантой в одну фазу, приспособительных механизмов. В результате процесса приспособления достигается возможный в данной ситуации максимум привыкания. Далее устойчивость организма либо длительно сохраняется на этом уровне, либо имеет волнообразное течение без существенных спадов. В тех случаях, когда повышение резистентности и поддержка этого состояния достигаются напряжением компенсаторно-защитных механизмов, могут развиваться сдвиги функций ряда систем и органов; могут развиваться и патологические явления как без срыва привыкания, так и с его срывом. Привыкание может быть нарушено усилением действующего фактора или действием другого агента, требующего иных приспособительных механизмов.
Третья фаза – выраженной интоксикации – не является обязательной. Она связана со срывом привыкания. Как правило, и срыву предшествует период напряженности адаптивных процессов, когда адаптационные механизмы все более заменяются компенсаторными. В таких случаях обнаружить напряженность можно, применяя либо экстремальные нагрузки, одинаковые для подопытных и контрольных животных (если говорить об экспериментальных условиях), либо наблюдая многие неспецифические показатели, которые иллюстрируют определенно нарастающие сдвиги. Срыв привыкания ведет к явной патологии, а пониженная чувствительность к основному агенту, вызвавшему привыкание, переходит в повышенную чувствительность к нему. Фаза выраженной интоксикации характеризуется наличием симптомов, специфичных для действующего яда.
Следует отметить, что фаза привыкания и в жизни, и в длительном эксперименте, как правило, прерывается периодами проявления интоксикации. Это связано с ослаблением компенсаторно-защитных механизмов либо вследствие перенапряжения (чаще при достаточно сильной интенсивности воздействия), либо с действием дополнительного фактора (например заболевания, переутомления). С течением времени периоды проявления интоксикации повторяются все чаще и становятся все длительнее и, наконец, завершаются полным переходом в третью фазу – фазу выраженной интоксикации.
Воздействие ионизирующего излучения на организм
Источниками внешнего облучения организма являются космическое излучение и естественные радионуклиды, содержащиеся в почве, воде и воздухе, а также рентгенодиагностические процедуры, цветные телевизоры и полеты на самолетах на больших высотах (хотя вклад двух последних факторов и невелик).
Каково соотношение внешнего и внутреннего облучения? Например, после Чернобыльской аварии в течение первых двух лет внешнее достигало 90 % от общей дозы, затем стало преобладать внутреннее облучение, достигшее к 1992 г. 80 %.
Природные радиоактивные элементы содержатся в строительных материалах, особенно в бетонных конструкциях. Плохая вентиляция, особенно в домах с плотно закрывающимися окнами, может увеличить дозу облучения, обусловленную вдыханием радиоактивных аэрозолей за счет распада газа радона, который образуется в свою очередь при естественном распаде радия, содержащегося в почве и строительных материалах. Использование в сельском хозяйстве фосфорных удобрений, содержащих естественные радионуклиды рядов урана и тория, является дополнительным фактором облучения организма человека. Эти радионуклиды накапливаются в почве, затем с пылью и продуктами питания попадают в организм. Могут выбрасывать в атмосферу радиоактивную золу тепловые электростанции. Облучение зависит от исходного сырья, условий его сгорания, эффективности золоулавливающих систем. Человек может получать некоторую дозу за счет газо-аэрозольных выбросов атомных электростанций и оседания на почву техногенных радионуклидов.
Стадия радиобиологических процессов, для которых характерны мутации в организме, называется биохимической.
Стадия радиобиологических процессов, для которой характерно образование первичных повреждений ДНК вследствие реакций со свободными радикалами, называется химической.
Стадия радиобиологических процессов, для которых характерно гибель клеток или изменение их свойств, в результате мутации, является биологической.
Эффекты воздействия ионизирующего излучения, которые проявляются спустя годы после излучения не только у непосредственно облученных лиц, но и у их потомства называется стохастическими. Стохастические эффекты воздействия ионизирующего излучения развиваются с момента облучения по прошествии десяти и более лет.
Степень воздействия ионизирующего излучения на органы и ткани человека оценивается поглощенной дозой.
Доза вещества, которая воздействует на популяцию или экосистему, называется экспозицией.
Выпадающие на поверхность почвы радионуклиды на протяжении многих лет остаются в ее верхних слоях. Если почвы бедны такими минеральными компонентами, как кальций, калий, натрий, фосфор, то создаются благоприятные условия для миграции радионуклидов в самих почвах и по цепи почва – растение. В первую очередь это относится к дерново-подзолистым и песчано-суглинистым почвам. Так, например, лишайники в тундре на почвах, бедных минеральными компонентами, захватывают цезий-137 в 200-400 раз больше, чем травы. Это обстоятельство способствует накоплению в организме северных оленей повышенного количества радионуклидов. В черноземных почвах подвижность радионуклидов крайне затруднена.
Аккумулятором радионуклидов является лес, особенно хвойный, который содержит в 5-7 раз больше радионуклидов, чем другие природные ценозы. При пожарах сконцентрированные в лесной подстилке, коре, древесине радионуклиды поднимаются с дымовыми частицами в воздух и попадают в тропосферу и даже стратосферу. Радиоактивному облучению, таким образом, подвергается население на значительных территориях. Пожары в Свердловской, Челябинской, Тюменской и Курганской областях только в 1989 г. дали 23 % всех лесных пожаров бывшего СССР.
Мало радиоактивных веществ поступает в рацион с пищевыми продуктами морского происхождения, так как из-за высокой минерализации морской воды продукты моря очень слабо загрязнены стронцием и цезием. Свободны от загрязнения радионуклидами глобальных выпадений артезианские и многие грунтовые воды, благодаря изоляции от поверхности земли. А вот воды подземных водоемов, талые и дождевые воды могут служить источником поступления некоторых радионуклидов в организм человека.
Исследования показали, что с вдыхаемым атмосферным воздухом человек может получать 1-2 % радионуклидов от их общего количества, поступающих с пищей и водой.
Хлебопродукты являются ведущим поставщиком радионуклидов в организм - от одной трети до половины их общего поступления. На втором месте по значимости находится молоко, на третьем – картофель, овощи и фрукты, затем мясо и рыба. Например, накопление радионуклидов у рыб разных пород даже в одном и том же водоеме может различаться в 2-3 раза. Для хищных рыб (щуки, окуня и др.) характерны минимальные показатели и накопления стронция-90 и максимальные – цезия-137. Растительноядные рыбы (карп, карась и др.) наоборот накапливают стронция больше, а цезия в несколько раз меньше, чем хищники. Наибольшие уровни накопления радионуклидов характерны для пресноводных рыб северных районов нашей страны, где воды поверхностных водоемов, особенно озер, слабоминерализованы.
На накопление радионуклидов в тканях рыб влияет тепловое загрязнение водоемов. Размещение рыбохозяйственных комплексов у мест удаления тепловых вод теплоэлектростанций и особенно АЭС способствует также более интенсивному усвоению и накоплению в тканях рыб находящихся в воде радионуклидов. Согласно данным, полученным в условиях лабораторных экспериментов, установлено, что уровни накопления цезия-137 в тканях карпа, обитавшего в воде с температурой 25 °С, вдвое выше, чем при обитании этой рыбы в воде с температурой 12-15 °С.
Из организма наиболее быстро выводятся радиоактивные вещества, концентрирующиеся в мягких тканях и внутренних органах: цезий, молибден, рутений, йод, теллур), медленно – прочно фиксированные в костях (стронций, плутоний, барий, иттрий, цирконий, ниобий, лантаноиды). Из большого числа радионуклидов наибольшую значимость как источник облучения населения представляет стронций-90 и цезий-137.
Стронций-90. Период полураспада этого радиоактивного элемента составляет 29 лет. При попадании стронция внутрь его концентрация в крови уже через 15 минут достигает значительной величины, а в целом этот процесс завершается через пять часов. Стронций избирательно накапливается, в основном, в костях и облучению подвергаются костная ткань, костный мозг, кроветворная система. Вследствие этого развивается анемия, называемая в народе «малокровием». Исследования показали, что радиоактивный стронций может находиться и в костях новорожденных. Через плаценту он проходит в течение всего периода беременности, причем, в последний месяц перед рождением в скелете его накапливается столько же, сколько аккумулировалось за все предыдущие восемь месяцев. Биологический период полувыведения стронция из скелета составляет свыше 30 лет. Ускорение выведения из организма стронция является труднейшей задачей. По крайней мере до сих пор не найдено высокоэффективных средств для быстрого выведения этого радиоактивного элемента из организма.
Цезий-137
После стронция-90 цезий-137 является самым опасным радионуклидом для человека. Он хорошо накапливается растениями, попадает в пищевые продукты и быстро всасывается в желудочно-кишечном тракте. Цезий-137 – долго живущий радионуклид, период его полураспада составляет 30 лет. До 80 % цезия откладывается в мышечной ткани. Биологические процессы эффективно влияют на цезий, поэтому в отличие от стронция биологический период полувыведения цезия у взрослых людей колеблется от 50 до 200 суток, у детей в возрасте 6-16 лет от 46 до 57 суток, у новорожденных – 10 суток. Причем, около 10 % нуклида быстро выводятся из организма, остальная часть – более медленными темпами. Но в любом случае ежегодное его содержание в организме практически определяется поступлением нуклида с рационом в данном году.
Радиоактивные вещества проникают в организм через легкие с вдыхаемым воздухом, через желудочно-кишечный тракт с зараженной водой и пищей, через раны и царапины на коже и даже через неповрежденную кожу. Радиоизотопы распределяются в организме неодинаково. Стронций, барий, радий накапливаются в скелете; лантаноиды, плутоний – в печени, селезенке, костном мозге; цезий, рубидий – в мышцах; рутений – в почках; радиоизотопы йода – в щитовидной железе. Попадая в организм, радионуклиды задерживаются там от нескольких дней до десятков лет.
Ядерная частичка, попадая в организм, действует там как мини реактор, воздействуя на клетки, и ее нужно вывести любыми средствами. Малые дозы облучения, согласно общепринятым в радиобиологии представлениям, не могут явиться причиной каких-либо непосредственных нарушений здоровья. Хотя согласно новейшим представлениям, даже санитарные нормативы, лимитирующие облучение, не гарантируют полной безопасности. Специалисты считают, что в связи с длительным воздействием даже самые малые дозы способны вызывать в клетках организма изменения, приводящие к генетическим нарушениям, злокачественным новообразованиям и разнообразным расстройствам обменных процессов организма, его пищеварительных, кроветворных и других функций. Могут быть другие неприятные последствия: ослабление сексуальной потребности, нарушение жизнеспособности потомства, раннее старение, уменьшение продолжительности жизни.
К ранним признакам лучевой болезни, по литературным данным, относятся чувство слабости и недомогания, головные боли и головокружение, повышенная возбудимость центральной нервной системы, бессонница. Нарушается пищеварение в виде потери аппетита и диспепсических жалоб (тошнота, рвота, тяжесть и боль под ложечкой, кишечные колики, нарушение стула), особенно у лиц более пожилого возраста. Часто наблюдается падение веса. Возможны функциональные расстройства сердечно-сосудистой деятельности, снижение кровеносного давления, нарушения деятельности почек, печени, повышение температуры, кровотечения.
Важно отметить, что ионизирующее излучение не воспринимается органами чувств человека: мы не видим его, не слышим и не чувствуем воздействия на наше тело. Радионуклиды постоянно попадая в организм, постепенно разрушают его, делая человека полубольным-полуздоровым.
Продукты, способствующие выведению из организма радионуклидов. Некоторые пищевые вещества обладают профилактическим радиозащитным действием или способностью связывать и выводить из организма радионуклиды. К ним относятся полисахариды (пектин, декстрин), фенильные и фитиновые соединения, галлаты, серотонин, этиловый спирт, некоторые жирные кислоты, микроэлементы, витамины, ферменты, гормоны. Радиоустойчивость организмов повышают некоторые антибиотики (биомицин, стрептомицин), наркотики (нембутал, барбамил).
Пектиновые вещества (пектин, пектиновая кислота). Пектин – студенистое вещество, которое хорошо заметно в варенье или желе, приготовленных из плодов. В процессе усвоения пищи пектин превращается в полигалактуроновую кислоту, которая соединяется с радионуклидами и токсичными тяжелыми металлами. Образуются нерастворимые соли, не всасывающиеся через слизистую желудочно-кишечного тракта и выделяющиеся из организма с калом. Кроме того, низкомолекулярные фракции пектина проникают в кровь, образуют с радионуклидами комплексы и затем удаляются с мочой. Пектиносодержащие вещества обладают высокой способностью в течение 1-3 часов связывать стронций, цезий, цирконий, рутений, иттрий, ионы свинца, лантана, ниобия и эвакуировать из организма до половины этих элементов.
Кроме пектина радиозащитным действием обладают и другие полисахариды типа декстрина, а также липополисахариды, находящиеся в листьях винограда и чая.
Выведению стронция из организма способствует кальций, которого особенно много в скорлупе перепелиных и куриных яиц.
Витамины. К очень важным радиозащитным соединениям относятся так называемые «витамины противодействия». В первую очередь это относится к витаминам группы В и С. Хотя по мнению специалистов одна аскорбиновая кислота не обладает защитным действием, но она усиливает действие витаминов В и Р.
В то время как радиоактивные элементы приводят к разрушению стенок кровеносных сосудов, совместное действие витаминов Р и С восстанавливает их нормальную эластичность и проницаемость. Радионуклиды разрушают кровь, снижают количество эритроцитов и активность лейкоцитов, а витамины В1, В3, В6, В12 улучшают регенерацию кроветворения, ускорение восстановления эритроцитов и лейкоцитов. Если излучение снижает свертываемость крови, то витамины Р и К1 нормализуют протромбиновый индекс.
Несколько повышает устойчивость организма к развитию лучевой болезни парааминобензойная кислота. Она улучшает показатели крови, способствует восстановлению веса и витамина Н.
Фенольные соединения растений ученые определяют как наиболее перспективные источники потенциально активных противолучевых средств. Фенольные соединения – это биологически активные вещества лечебно-профилактического действия, необходимые для поддержания жизни и сохранения здоровья. Они повышают прочность кровеносных сосудов, регулируют работу желез внутренней секреции. Например, хорошо лечит местные лучевые повреждения кожи прополис (пчелиный клей), что главным образом связано с его фенольными компонентами. Из многочисленного ряда фенольных веществ наибольший интерес вызывают флавоноиды, способствующие удалению радиоактивных элементов из организма. Источниками флаваноидов являются мандарины, черноплодная рябина, облепиха, боярышник, пустырник, бессмертник и солодка.
Наркомания причины и последствия
Наркомания (от греч. «narкe» оцепенение, сон и «mania» безумие, страсть, влечение), (синоним – токсикомания) – это патологическое пристрастие к наркотическим веществам, действующим преимущественно на центральную нервную систему. Наркомания характеризуется непреодолимой потребностью к повтрным приемам все увеличивающихся доз наркотических веществ. При отсутствии преперата наблюдается абсистенция. Она характеризуется разбитостью, бессонницей, сильными болями в суставах, ломотой во всем теле, головной болью тошнотой, рвотой. При длительном употреблении наркотиков возникают отчетливые изменения личности. Интересы больного поглощаются только необходимостью добыть наркотики. Пояляется лживость, исчезает интерес к труду, любовь к близким, родным. Нередко больные совершают правонарушения и преступления.
Выделяют опийную наркоманию; наркоманию, обусловленную злоупотреблением препаратов конопли; наркоманию, вызванную злоупотреблением эфедрина; барбитуровую и кокаиновую наркомании; наркоманию, вызываемую галлюциногенами типа ЛСД.
ЛСД (диэтиламид лизергиновой кислоты) – полусинтетическое вещество, производное лизергиновой кислоты, извлеченное из гриба спорыньи ржи. ЛСД, далеко не самый последний потомок семьи наркотиков, появившись в 60-е годы прошлого века, он открыл путь еще более сильнодействующим веществам. Чтобы понять опасность, которую несет с собой такой взрыв наркотиков, напомним, что достаточно принять миллионную долю грамма ЛСД на каждый килограмм веса, чтобы он стал галлюциногировать.
Злоупотребление наркотиками, известное с древнейших времен, сейчас распространилось в размерах, тревожащих всю мировую общественность. Даже при сужении, с точки зрения наркологов, границ наркомании до юридических приемлемых во многих странах наркомании признаны социальным бедствием.
Современные ученые достаточно подробно разрабатывают объяснения возникновения наркотической зависимости и выделяют 3 основных направления:
1. социологические, включающие влияние общества и семьи,
2. биологические, объясняющие склонности к злоупотреблению особенностями организма и особой предрасположенностью,
3. психологические, рассматривающие особенности и отклонения в психике.
Социальные факторы
Общественные неурядицы, потери работы, жилья, социальная неустроенность часто приводит людей к употреблению наркотиков.
Психологические факторы
Благоприятным поводом попробовать наркотики становятся эмоциональные расстройства, депрессии, потребность выровнять настроение. Способность седятивных (успокоительных) и психоделяческих наркотиков снимать тревогу, подавленность, напряжение, раздражительность побуждает их использовать как средство от депрессии. В ее тяжелых формах употребление наркотиков становится выражением стремления к самоуничтожению медленным самоубийством. Если сначала наркотик «работает» средством от депрессии, то спустя очень короткий срок сам становится ее источникам. Частота депрессий резко увеличивается особенно в подростковом возрасте.
Биологические факторы
Различные люди по-разному реагируют на токсические и биологические воздействия. В эпидемию заболевают не все, при массовых отравлениях некоторые остаются здоровы. Люди по- разному переносят жару и холод. Наркотическая зависимость тоже развивается далеко не у всех. Пробуют наркотики гораздо больше людей, чем заболевают наркоманией. Однако особо предрасположенные к тому или иному веществу заболевают наркоманией с первого раза.
Все случаи употребления наркотиков можно часто объединить одной целью – стремлению к удовольствию. Именно поиск удовольствия заставляет увеличивать дозу по мере привыкания организма для достижения все более сомнительной эйфории, приводя к необратимой зависимости от употребляемого яда. Эйфория гаснет с каждым разом, заставляя принимать «ударные дозы», приводящей к невозможности существования без вещества, ставшего необходимым компонентом жизнедеятельности по-новому устроенного организма. Единственным средством избежать гибели, если человек употребляет наркотик, но еще не впал в физическую зависимость, является самоконтроль и знание тяжелейших последствий злоупотребления наркотиков.
Необходим контроль над производством и продажей наркотиков, проведение разьяснительной работы об опасности и тяжелых последствиях приема наркотиков.


